„Fajhő mérése” változatai közötti eltérés
| 102. sor: | 102. sor: | ||
A ''2. ábra'' a kaloriméteres mérés során a kaloriméter hőmérsékletének változását mutatja be az idő függvényében. A görbe három jól elkülöníthető szakaszra osztható, az egyes szakaszokon lejátszódó folyamatokat áttekintjük: | A ''2. ábra'' a kaloriméteres mérés során a kaloriméter hőmérsékletének változását mutatja be az idő függvényében. A görbe három jól elkülöníthető szakaszra osztható, az egyes szakaszokon lejátszódó folyamatokat áttekintjük: | ||
| − | * ''Előperiódus'': A kaloriméterbe helyezett folyadék (víz, olaj stb.) és a kaloriméter, valamint a folyadék és a környezet közötti hőmérsékleti egyensúly kialakulásának folyamata. A kaloriméter és a mérő folyadék hőmérsékletétől függően ebben a szakaszban a belső tér hőmérséklete csökken ha $t_{b0} > t_0$ vagy növekszik ha $t_{b0} < t_0$ ($t_{b0}$ a belső tér hőmérséklete kísérlet indításakor). | + | * ''Előperiódus'': A kaloriméterbe helyezett folyadék (víz, olaj stb.) és a kaloriméter, valamint a folyadék és a környezet közötti hőmérsékleti egyensúly kialakulásának folyamata. A kaloriméter és a mérő folyadék hőmérsékletétől függően ebben a szakaszban a belső tér hőmérséklete csökken ha $t_{b0} > t_0$ vagy növekszik ha $t_{b0} < t_0$ ($t_{b0}$ a belső tér hőmérséklete kísérlet indításakor). Ebben a szakaszban a kis hőmérsékletkülönbségek miatt a hőmérséklet - idő kapcsolat jó közelítéssel lineárisnak tekinthető. |
| − | Ebben a szakaszban a kis hőmérsékletkülönbségek miatt a hőmérséklet - idő kapcsolat jó közelítéssel lineárisnak tekinthető. | + | |
* ''Főperiódus'': Az előperiódus a fő energiaátadási folyamattal folytatódik (főperiódus), amely az anyagok összekeveredésével illetve a fűtőtest bekapcsolásával kezdődik. A főperiódusban a belső tér hőmérséklete ($t_b$) emelkedik. Ebben a szakaszban megy végbe az energiacsere az összekevert különböző hőmérsékletű anyagok között, vagy a kaloriméterben levő anyagok és a fűtőtest között. A kaloriméter belsejének hőmérséklete a környezeti hőmérséklet fölé emelkedik $t_{b} > t_0$ és ezért energialeadás történik a környezet felé. A hőveszteség miatt a belső tér hőmérséklete nem érheti el a tökéletes hőszigetelés esetén várható $t_k$ egyensúlyi hőmérsékletet. A főperiódust követő szakasz (az utóperiódus) hőmérséklet-idő grafikonjából azonban következtetni tudunk erre az értékre. | * ''Főperiódus'': Az előperiódus a fő energiaátadási folyamattal folytatódik (főperiódus), amely az anyagok összekeveredésével illetve a fűtőtest bekapcsolásával kezdődik. A főperiódusban a belső tér hőmérséklete ($t_b$) emelkedik. Ebben a szakaszban megy végbe az energiacsere az összekevert különböző hőmérsékletű anyagok között, vagy a kaloriméterben levő anyagok és a fűtőtest között. A kaloriméter belsejének hőmérséklete a környezeti hőmérséklet fölé emelkedik $t_{b} > t_0$ és ezért energialeadás történik a környezet felé. A hőveszteség miatt a belső tér hőmérséklete nem érheti el a tökéletes hőszigetelés esetén várható $t_k$ egyensúlyi hőmérsékletet. A főperiódust követő szakasz (az utóperiódus) hőmérséklet-idő grafikonjából azonban következtetni tudunk erre az értékre. | ||
A lap 2012. augusztus 29., 00:38-kori változata
Szerkesztés alatt!
A mérés célja:
- elmélyíteni a hallgatók fajhővel kapcsolatos ismereteit,
- megismertetni a hallgatókat a fajhőmérés két módszerével.
Ennek érdekében:
- összefoglaljuk a fajhő mérésével kapcsolatos ismereteket, ismertetjük a keverési kaloriméterrel ill. az elektromos fűtésű kaloriméterrel történő fajhőmérést,
- a gyakorlat során megmérjük néhány anyag fajhőjét.
Tartalomjegyzék[elrejtés] |
Elméleti összefoglaló
Egy anyag belső energiája (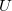 ) a rajta végzett makroszkopikus munka (
) a rajta végzett makroszkopikus munka (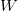 ), vagy egy másik testtel létrejött kontaktus során molekuláris szinten lezajló energia átadás (
), vagy egy másik testtel létrejött kontaktus során molekuláris szinten lezajló energia átadás (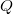 ) útján változtatható meg. Ezt a tapasztalatot rögzíti a hőtan I. főtétele:
) útján változtatható meg. Ezt a tapasztalatot rögzíti a hőtan I. főtétele:
![\[ \Delta U = \Delta Q + \Delta W \]](/images/math/2/7/f/27f7ad7ea1ba2b5b9574422f9502787f.png)
ahol 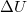 a belső energia megváltozása,
a belső energia megváltozása, 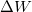 a testen végzett makroszkopikus munka,
a testen végzett makroszkopikus munka, 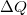 pedig a molekuláris mechanizmussal a testnek átadott energia, amit hőnek (hőmennyiségnek) nevezünk. Ha egy testtel hőt közlünk (pl. elektromos fűtőtesttel melegítjük), akkor belső energiája és ezzel együtt hőmérséklete is megváltozik. A tapasztalat szerint nem túl nagy hőmennyiség közlése esetén a bekövetkező hőmérséklet-változás (
pedig a molekuláris mechanizmussal a testnek átadott energia, amit hőnek (hőmennyiségnek) nevezünk. Ha egy testtel hőt közlünk (pl. elektromos fűtőtesttel melegítjük), akkor belső energiája és ezzel együtt hőmérséklete is megváltozik. A tapasztalat szerint nem túl nagy hőmennyiség közlése esetén a bekövetkező hőmérséklet-változás (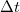 ) egyenesen arányos a közölt hővel (
) egyenesen arányos a közölt hővel (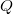 ), fordítottan arányos a vizsgált anyag tömegével (
), fordítottan arányos a vizsgált anyag tömegével (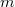 ) és függ a vizsgált anyag minőségétől is:
) és függ a vizsgált anyag minőségétől is:
![\[ \Delta t = \frac{Q}{cm} \]](/images/math/d/a/c/dac3f1f9b1083257be4bfc9306623ef2.png)
ahol az anyagra jellemző  állandót fajhőnek nevezzük. Számértéke megadja, hogy egységnyi tömegű anyaggal mennyi hőt kell közölnünk ahhoz, hogy hőmérsékletét 1 K-nel megváltoztassuk. Mértékegysége
állandót fajhőnek nevezzük. Számértéke megadja, hogy egységnyi tömegű anyaggal mennyi hőt kell közölnünk ahhoz, hogy hőmérsékletét 1 K-nel megváltoztassuk. Mértékegysége 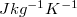 .
.
A testtel közölt hő azonban nemcsak a belső energia megváltoztatására, hanem munkavégzésre is fordítódhat:
![\[ \Delta Q = \Delta U - \Delta W \]](/images/math/1/3/6/13659aec3eb30ac8afa0da477615ebec.png)
Ennek megfelelően a fajhő:
![\[ c = \frac{1}{m} \frac{\Delta Q}{\Delta t} = \frac{1}{m} \frac{\Delta U}{\Delta t} - \frac{1}{m} \frac{\Delta W}{\Delta t} \]](/images/math/2/e/7/2e74705f7fc63f133db52e5666b153ec.png)
Mivel a munkavégzés függ a folyamat körülményeitől, a fajhő csak akkor határozható meg egyértelműen, ha a hőközlés folyamatát pontosan rögzítjük. Ennek megfelelően, elvileg igen sokféle fajhő definiálható, a gyakorlatban ezek közül kettőt használnak, az állandó térfogaton (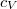 ) és az állandó nyomáson (
) és az állandó nyomáson (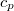 ) mért fajhőt. Gázok esetében e kétféle fajhő számottevően különböző, szilárd és folyékony anyagoknál közel azonos értékű.
) mért fajhőt. Gázok esetében e kétféle fajhő számottevően különböző, szilárd és folyékony anyagoknál közel azonos értékű.
A fajhő – különösen alacsony hőmérsékleten – a hőmérséklettől is függ. A mérés során szilárd anyagokat vizsgálunk amelyeknek fajhője a vizsgált hőmérsékleteken állandónak tekinthető és amelyeknél a 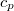 és
és 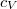 eltérése is elhanyagolható. Ezért a továbbiakban egyszerűen "fajhő"-ről beszélünk és az index nélküli
eltérése is elhanyagolható. Ezért a továbbiakban egyszerűen "fajhő"-ről beszélünk és az index nélküli  jelölést használunk. (Szigorúan véve
jelölést használunk. (Szigorúan véve 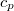 -t mérjük.)
-t mérjük.)
A mérnöki gyakorlatban a hűtő- és fűtő berendezések és határoló szerkezetek hőtani viselkedésének egyik meghatározója az alkalmazott anyagok fajhője. Az anyagtudományban a fajhő mérésével bizonyos anyagszerkezeti változásokat – fázisátalakulásokat – követhetünk nyomon. A fajhő meghatározása a 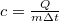 képlet alapján lehetséges. Megmérve a vizsgált anyag tömegét, az anyaggal közölt ill. a tőle elvont hő mennyiségét és a bekövetkezett hőmérsékletváltozást, a fajhő kiszámítható.
képlet alapján lehetséges. Megmérve a vizsgált anyag tömegét, az anyaggal közölt ill. a tőle elvont hő mennyiségét és a bekövetkezett hőmérsékletváltozást, a fajhő kiszámítható.
A gyakorlatban sok esetben közvetlenül a testtel közölt hő és a hőmérsékletváltozás összefüggésére van szükség, így a fajhő helyett az adott testre jellemző 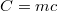 mennyiséget használják, amelyet hőkapacitásnak neveznek. A
mennyiséget használják, amelyet hőkapacitásnak neveznek. A 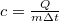 összefüggés így a
összefüggés így a 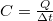 alakot ölti.
alakot ölti.
A vizsgált anyaggal történő hőközlés két módszere terjedt el, a különböző hőmérsékletű anyagok összekeverésével ill. az elektromos fűtőtesttel történő hőközlés. Az alábbiakban ezen két módszer alapgondolatát ismertetjük.
Fajhőmérés keveréssel
A mérendő  fajhőjű,
fajhőjű, 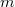 tömegű,
tömegű, 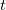 hőmérsékletű anyagot ismert paraméterekkel (
hőmérsékletű anyagot ismert paraméterekkel (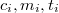 ) rendelkező anyaggal – általában olyan folyadékkal, amely nem lép kémiai reakcióba a mérendő anyaggal – összekeverjük, majd megmérjük a beálló közös hőmérsékletet (
) rendelkező anyaggal – általában olyan folyadékkal, amely nem lép kémiai reakcióba a mérendő anyaggal – összekeverjük, majd megmérjük a beálló közös hőmérsékletet (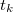 ). Feltéve, hogy a keverés során a két anyag között kizárólag hőátadás történik, a vizsgálandó anyag által felvett (vagy leadott) hő egyenlő az ismert anyag által felvett (vagy leadott) hővel, ezért
). Feltéve, hogy a keverés során a két anyag között kizárólag hőátadás történik, a vizsgálandó anyag által felvett (vagy leadott) hő egyenlő az ismert anyag által felvett (vagy leadott) hővel, ezért
![\[ c m ( t - t_k ) = c_i m_i ( t_k - t_i ) \]](/images/math/4/1/3/413b0e7bcec89bad57cd8e555aaa6052.png)
ami alapján az ismeretlen  fajhő meghatározható.
fajhő meghatározható.
Ez a módszer elsősorban szilárd testek és folyadékok fajhőjének meghatározására alkalmas, de segítségével gázok állandó nyomáson mért fajhője is megmérhető. Ebben az esetben a vizsgált gázt cső-spirálon áramoltatják a folyadékon át. A gáz tömegének, hőmérsékletváltozásának valamint a mérő folyadék adatainak ismeretében a gáz állandó nyomáson mért fajhője (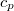 ) meghatározható. Az állandó nyomáson mért fajhő ismeretében az állandó térfogaton mért fajhő, (
) meghatározható. Az állandó nyomáson mért fajhő ismeretében az állandó térfogaton mért fajhő, (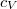 ) szintén meghatározható (pl. hangsebesség-méréssel).
) szintén meghatározható (pl. hangsebesség-méréssel).
Fajhőmérés elektromos energiaközléssel
Ennél a módszernél a vizsgált anyag (fajhője  , tömege
, tömege 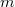 ) hőmérsékletét elektromos fűtőtest segítségével
) hőmérsékletét elektromos fűtőtest segítségével 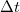 értékkel megnöveljük. Feltéve, hogy a fűtőtest által leadott energia teljes egészében a vizsgált anyag belső energiáját növeli:
értékkel megnöveljük. Feltéve, hogy a fűtőtest által leadott energia teljes egészében a vizsgált anyag belső energiáját növeli:
![\[ U I \tau = c m \Delta t \]](/images/math/e/a/4/ea447715765cb9f8f91c3f70d4c7b62f.png)
amiből az UI fűtőteljesítmény, a  melegítési idő, a vizsgált anyag
melegítési idő, a vizsgált anyag 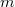 tömege és a
tömege és a 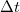 hőmérsékletváltozás ismeretében a
hőmérsékletváltozás ismeretében a  fajhő meghatározható.
fajhő meghatározható.
A módszer elsősorban folyadékok fajhőjének meghatározására alkalmas. Használható azonban szilárd anyagok esetén is, ha azokat folyadékba helyezve a folyadékkal együtt melegítjük.
A kaloriméter hőkapacitása és a hőmérsékleti korrekció
A keveréssel és az elektromos melegítéssel történő fajhőmérés esetén eddig feltételeztük, hogy a folyamat a környezettől hőtanilag jól elszigetelve, hőveszteség nélkül játszódik le. Ennek a feltételnek a teljesítése érdekében a hőközlés a környezettől jó hőszigetelő anyagokkal elválasztott edényben, kaloriméterben történik. (Egy keverési és egy elektromos kaloriméter vázlatát az 1. ábra mutatja.)
Ennek ellenére a hőveszteség nélküli mérés mégsem valósítható meg, elsősorban az alábbi két ok miatt: az egyik az, hogy az edény hőmérséklete is változik a mérés közben és ez is energiát igényel, a másik pedig, hogy bármilyen jó hőszigetelést is alkalmazunk a környezet felé mindig történik energiaátadás. Ez a két ok (hiba) a kaloriméter hőkapacitásának figyelembevételével illetve a hőveszteségek becslésével csökkenthető.
A kaloriméter hőkapacitása
Ha tudnánk azt, hogy a kaloriméter egyes részei milyen tömegűek, mekkora a fajhőjük és milyen mértékben melegszenek fel, akkor meg tudnánk határozni a kísérlet közben a kaloriméter egyes részeinek melegítéséhez szükséges energiát. Ez az eljárás gyakorlatilag megvalósíthatatlan. Ehelyett mérés segítségével meghatározzuk a kaloriméter 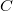 hőkapacitását. Ha a kaloriméter hőkapacitását is figyelembe vesszük, akkor a hőcserét leíró egyenleteink az alábbiak szerint módosulnak:
hőkapacitását. Ha a kaloriméter hőkapacitását is figyelembe vesszük, akkor a hőcserét leíró egyenleteink az alábbiak szerint módosulnak:
![\[ c m ( t - t_k ) = c_i m_i ( t_k - t_i ) + C ( t_k - t_i )\]](/images/math/c/f/5/cf598a2aa784520a46a17534ddcd6899.png)
![\[ U I \tau = c m \Delta t + C \Delta t. \]](/images/math/d/6/4/d64af22861d66fd1ceace71d63ee76ce.png)
A kaloriméter hőkapacitásának meghatározásához ismert fajhőjű (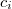 ,
,  ) anyagok alkalmazásával a fenti egyenletek valamelyikével történik. Ismert fajhőjű anyagként rendszerint vizet alkalmazunk.
) anyagok alkalmazásával a fenti egyenletek valamelyikével történik. Ismert fajhőjű anyagként rendszerint vizet alkalmazunk.
A hőmérsékleti korrekció
A kaloriméter belseje és a környezet között energiaátadást a belső tér (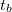 ) és a környezet (
) és a környezet (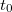 ) hőmérséklete közötti eltérés eredményezi. Az ezen hőmérsékletkülönbség okozta energiaátadást jó hőszigeteléssel valamint egymáshoz közeli
) hőmérséklete közötti eltérés eredményezi. Az ezen hőmérsékletkülönbség okozta energiaátadást jó hőszigeteléssel valamint egymáshoz közeli 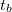 és
és 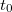 választással csökkentjük. A kaloriméter belseje és a külső tér között mindezek ellenére fellépő energiacsere "hőmérsékleti korrekcióval" vehető figyelembe. Az alábbiakban a hőmérsékleti korrekció grafikus végrehajtását mutatjuk be.
választással csökkentjük. A kaloriméter belseje és a külső tér között mindezek ellenére fellépő energiacsere "hőmérsékleti korrekcióval" vehető figyelembe. Az alábbiakban a hőmérsékleti korrekció grafikus végrehajtását mutatjuk be.
A 2. ábra a kaloriméteres mérés során a kaloriméter hőmérsékletének változását mutatja be az idő függvényében. A görbe három jól elkülöníthető szakaszra osztható, az egyes szakaszokon lejátszódó folyamatokat áttekintjük:
- Előperiódus: A kaloriméterbe helyezett folyadék (víz, olaj stb.) és a kaloriméter, valamint a folyadék és a környezet közötti hőmérsékleti egyensúly kialakulásának folyamata. A kaloriméter és a mérő folyadék hőmérsékletétől függően ebben a szakaszban a belső tér hőmérséklete csökken ha
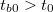 vagy növekszik ha
vagy növekszik ha 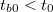 (
(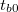 a belső tér hőmérséklete kísérlet indításakor). Ebben a szakaszban a kis hőmérsékletkülönbségek miatt a hőmérséklet - idő kapcsolat jó közelítéssel lineárisnak tekinthető.
a belső tér hőmérséklete kísérlet indításakor). Ebben a szakaszban a kis hőmérsékletkülönbségek miatt a hőmérséklet - idő kapcsolat jó közelítéssel lineárisnak tekinthető.
- Főperiódus: Az előperiódus a fő energiaátadási folyamattal folytatódik (főperiódus), amely az anyagok összekeveredésével illetve a fűtőtest bekapcsolásával kezdődik. A főperiódusban a belső tér hőmérséklete (
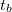 ) emelkedik. Ebben a szakaszban megy végbe az energiacsere az összekevert különböző hőmérsékletű anyagok között, vagy a kaloriméterben levő anyagok és a fűtőtest között. A kaloriméter belsejének hőmérséklete a környezeti hőmérséklet fölé emelkedik
) emelkedik. Ebben a szakaszban megy végbe az energiacsere az összekevert különböző hőmérsékletű anyagok között, vagy a kaloriméterben levő anyagok és a fűtőtest között. A kaloriméter belsejének hőmérséklete a környezeti hőmérséklet fölé emelkedik 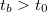 és ezért energialeadás történik a környezet felé. A hőveszteség miatt a belső tér hőmérséklete nem érheti el a tökéletes hőszigetelés esetén várható
és ezért energialeadás történik a környezet felé. A hőveszteség miatt a belső tér hőmérséklete nem érheti el a tökéletes hőszigetelés esetén várható 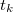 egyensúlyi hőmérsékletet. A főperiódust követő szakasz (az utóperiódus) hőmérséklet-idő grafikonjából azonban következtetni tudunk erre az értékre.
egyensúlyi hőmérsékletet. A főperiódust követő szakasz (az utóperiódus) hőmérséklet-idő grafikonjából azonban következtetni tudunk erre az értékre.
- Utóperiódus: Ebben a szakaszban
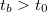 és a nem tökéletes hőszigetelés miatt lassan csökken a kaloriméter belsejében a hőmérséklet. A hőmérsékletcsökkenést most is lineárisnak tekintjük.
és a nem tökéletes hőszigetelés miatt lassan csökken a kaloriméter belsejében a hőmérséklet. A hőmérsékletcsökkenést most is lineárisnak tekintjük.
Látható, hogy a folyamat a nem tökéletes hőszigetelésből adódó hibák miatt az ideálistól eltérően alakul. A hőmérséklet - idő görbe felvétele azonban lehetőséget ad a hibák korrigálására. A hőmérsékleti korrekció gyakorlati végrehajtása a következőképpen történik (2. ábra). Felvesszük a kaloriméter hőmérsékletének időfüggvényét. Az elő- és utóperiódus szakaszára egyenest illesztünk. Tegyük fel, hogy az előperiódusra illesztett egyenes utolsó érintési pontjának koordinátái 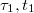 . Az utóperiódusra illesztett egyenes első érintkezési pontjának koordinátái
. Az utóperiódusra illesztett egyenes első érintkezési pontjának koordinátái 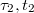 . Ezek megállapítása után megrajzoljuk a
. Ezek megállapítása után megrajzoljuk a 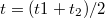 időtengellyel párhuzamos egyenest. Ennek az egyenesnek és a főperiódus görbéjének metszéspontján keresztül párhuzamost húzunk a hőmérséklettengellyel. Ez utóbbi egyenesnek és az időperiódusra illesztett egyenesnek a metszéspontját tekintjük a kaloriméter + mérőfolyadék rendszer kezdeti hőmérsékletének (
időtengellyel párhuzamos egyenest. Ennek az egyenesnek és a főperiódus görbéjének metszéspontján keresztül párhuzamost húzunk a hőmérséklettengellyel. Ez utóbbi egyenesnek és az időperiódusra illesztett egyenesnek a metszéspontját tekintjük a kaloriméter + mérőfolyadék rendszer kezdeti hőmérsékletének (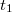 ), az utóperiódusra illesztett egyenessel való metszéspontját fogadjuk el közös hőmérsékletnek (
), az utóperiódusra illesztett egyenessel való metszéspontját fogadjuk el közös hőmérsékletnek (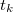 ).
).
A korrekció fenti módon történő végrehajtása az alábbiakon alapul: A környezettel való energiacsere miatt a kaloriméterben állandóan változik a hőmérséklet, egyensúlyi hőmérséklet sem alakulhat ki, így sem a kiindulási, sem a véghőmérsékletet nem tudjuk megmérni. Az előperiódusra fektetett egyenes mutatja, hogy hogyan változna a kaloriméter belsejében a hőmérséklet, ha nem indulna meg az energiacsere a főperiódusban. Ebből lehet a valódi kezdeti hőmérsékletre következtetni.
Az utóperiódusra fektetett egyenes segítségével arra lehet következtetni, hogy milyen hőmérséklet értéket vehetett volna fel a kaloriméter belseje ideális hőszigetelés mellett.
A jó minőségű kaloriméter hőkapacitása kicsi és hőszigetelése jó, azaz kicsi a környezettel való energiacsere. Ekkor a hőmérséklet közel állandó az elő- és utóperiódus során.