Lézerindukált fluoreszcencia mérése
Tartalomjegyzék[elrejtés] |
Szerkesztés alatt!
Elméleti összefoglaló
Bevezetés
Előszóként egy egyszerű kísérlet
Vegyünk egy zöld szobanövényt, pl. könnyező pálmát (Monstera deliciosa), egy diavetítőt, melynek lencséje elé a fény kék spektrális komponenseit széles sávban (pl.400-500 nm) áteresztő szűrőt helyeztünk, egy további, a 690 és 730 nm közötti spektrális komponenseket, áteresztő szűrőt és végül egy sötét takarót. Fedjük le a növény egyik levelét néhány percre (pl. 5-10 perc) a takaróval úgy, hogy elzárjuk a természetes fény elől. A takarót levéve hirtelen világítsuk meg a növény levelét a kék szűrőn át a vetítő fényével, és közben figyeljük a levelet a piros szűrőn keresztül. Ha eszközeink megfelelőek voltak, és a levelet előzetesen jól elzártuk a fény elől, akkor azt tapasztaljuk, hogy a megvilágítás helyén a levél erősen felfénylik, -sugározni kezd-, majd a sugárzás mértéke néhány perc elteltével visszaesik és egy alacsonyabb intenzitás értéknél, stabilizálódik. A jelenség -melynek neve Kautsky-effektus- annál erősebb, minél nagyobb fényintenzitású forrást használunk, illetve minél jobban és hosszabban tartottuk sötétben a növényt. Egyszerűsített magyarázata röviden az, hogy a sötétítés ideje alatt a levélben átmenetileg megszűnt a fotoszintézis fotokémiai folyamata és annak feltételei. A hirtelen megvilágítás hatására a level klorofillmolekulái a fényt azonnal kezdik elnyelni, ám mivel a fotoszintézis optimális feltételei csak lassabban alakulnak ki, ezért az eleinte elnyelt fény energiájának csak kisebb hányadát hasznosítja a klorofill a fotoszintézis táplálására, míg nagyobb részét kénytelen fluoreszcencia fény formájában visszasugározni. Később, - ahogy a fotoszintézis folyamata feléled-, az elnyelt fényt nagyobb hatásfokkal hasznosítja a levél és a fluoreszcencia fény lecsökken. A Kautsky-effektus időbeli lefolyását (kinetikáját) regisztráló un. „időfelbontásos klorofill fluorométereket” ma már széles körben alkalmazzák a biológusok a fotoszintézis és a növényi stressz-hatások kutatására és a növények állapotának jellemzésére.
Hallgatói mérésünk célja a fluoreszcencia jelenségének tanulmányozására szolgáló optikai, spektroszkópiai, optoelektronikai eszközök és mérési módszerek megismerése, kezelésük elsajátítása. Hangsúlyozzuk, hogy nem célunk a fotoszintézis és a klorofillfluoreszcencia (élő növényeken tapasztalt) működésének leírása, a folyamatok kapcsolatának pontos elemzése. Ez a növényélettannal foglalkozó biológusok feladata és ők jelenleg is intenzíven kutatnak e téren. Erre vonatkozó érdeklődés esetén indulásként javasoljuk az [1] , [2] irodalmak tanulmányozását.
A fluoreszcencia és a fluoreszcencia spektroszkópia
Fluoreszcenciáról beszélünk, ha egy fénnyel besugárzott molekula a fényelnyelést követően a besugárzó fényénél hosszabb hullámhosszon (alacsonyabb energián) fényt emittál. A fluoreszcenciát létrehozó fény hullámhossz (energia) szerinti eloszlását gerjesztési, míg a kisugárzottét emissziós spektrumnak nevezzük.
Egy általános fluoreszcencia spektroszkóp tehát lényegében két spektrumfelbontó elemet tartalmaz: egyet a gerjesztő fény, másikat az emittált fény komponensekre bontására (lásd 1. ábra).
| Fájl:Fluoreszcencia spektroszkóp felépítése.JPG Fluoreszcencia spektroszkóp felépítése 1. ábra |
Bevezető kísérletünkben a fény hullámhossz szerinti szelektálását interferenciaszűrőkkel valósítottuk meg. A gyakorlatban számtalan konfigurációval valósítanak meg fluoreszcencia spektroszkópokat, így fényforrásként (zárójelben a sugárzási tartomány)
- halogénlámpák (látható, közeli, infravörös),
- xenonlámpák (látható, ultraibolya),
- deutérium lámpák (ultraibolya),
- hangolható lézerek, pl. festéklézer ( látható);
monokromátorként:
- rácsok,
- hangolható akusztooptikai szűrők,
- prizmák,
- interferenciaszűrők;
detektorként:
- szilícium-fényérzékelők (látható, közeli infravörös),
- fotoelektronsokszorozók (látható, UV,közeli, infravörös),
- ólomszulfid(-szelenid) fotoellenállások (közeli infravörös),
- detektorsorok, pl.:
- - Si-alapú, CCD vagy diódasor (látható, közeli infravörös),
- - InGaAs diódasor (közeli infravörös)
alkalmazhatók.
A fluoreszcencia spektroszkópia alkalmazása széleskörű. Rendkívüli jelentősége, hogy roncsolásmentes, így az élő tudományok egyik jelentős in-situ vizsgálati módszerévé vált. Alkalmazható egyrészt direkt vizsgálatokra, (pl. energiaszintek mérésére, élettartamok meghatározására), de rendkívül széleskörű az alkalmazása indirekt vizsgálatokban, ahol a vizsgálandó molekulákat fluoreszcens molekulák segítségével színezik és ily módon jelenítik meg azokat.
Hallgatói mérésünkben egyrészt növényi leveleket nitrogén lézerrel gerjesztjük, és a vevőoldalon rács segítségével bontjuk fel, és szilícium detektorsorral detektáljuk az emittált fluoreszcencia fényt. Másrészt egy nitrogén lézer által pumpált, rács segítségével hangolt festéklézer emissziós spektrumát vizsgáljuk.
A vizsgálandó minta fluoreszcens jellemzői
Élő növények fluoreszcencia vizsgálata viszonylag rövid múlttal bíró tudományterület. Kautsky & Hirsch először 1934-ben írták le az élő növényekben lévő klorofill molekulák fluoreszcens fénykibocsátásának jellemzőit [3] . A festéklézert 1966-ban Sorokin és Lankard fedezte fel. Egy rubinlézer fényét egy fluoreszcens anyagot tartalmazó küvettára juttatta[4] .
A klorofillfluoreszcencia gerjesztése
A levél látható tartományban elnyelő összetevői a klorofillok és a karotenoidok. Izolált állapotukban az abszorpciós spektrumukat a 2. ábrán mutatjuk be. A 400-500 nm-es tartományban mindkét molekulacsalád fényelnyelő, 500 és 600 nm között jelentősen lecsökken az abszorpciójuk, majd a klorofilloké 600 nm fölött ismét megnő. A karotenoidok továbbra sem abszorbeálnak.
A klorofillfluoreszcencia sugárzási spektruma élő levélben
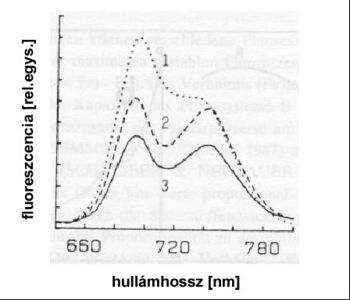
Lucfenyőtűk tipikus klorofillfluoreszcencia spektrumai láthatók a 3. ábrán. Jól látható, hogy a különböző klorofilltartalmú tűlevelek spektrumai különböznek egymástól.
Lényegében a spektrumra a tartomány (640-800 nm) és a két csúcs (690 nm és 740 nm) karakteres. A csúcsok viszonya, a köztük lévő völgy mélysége és azok időbeli változása egyrészt egyedfüggő, másrészt jellemzik a levél fotoszintetikus aktivitását, így a növénybiológusok kutatási területét képezik.
Levélfluoreszcencia UV gerjesztésre
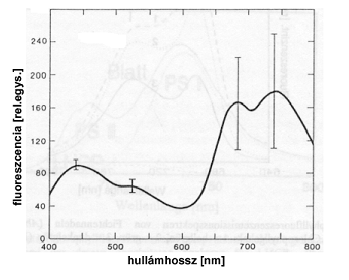
UV sugárzás hatására a klorofillra jellemző, 650-800 nm-es tartományban kisugárzott fluoreszcencia fényen kívül egy további, széles sávú (400-600 nm) emisszió tapasztalható.
A 450 nm körüli maximum (kék fluoreszcencia) és egy 530 nm körüli „váll” (zöld fluoreszcencia) jellemzik (lásd 4. ábrát). Pontos eredetük jelenleg is kutatás tárgyát képezik.
Az alkalmazott fluoreszcencia spektroszkóp és elemeinek ismertetése
Felépítés és működés
A vizsgálat impulzusüzemben történik, mivel az ultraibolya tartományban működő N2-lézer impulzusüzemű. UV gerjesztéskor csak a nitrogén lézer világítja meg a mintát, míg a látható tartományban csak a festéklézer. A nitrogén lézer ilyenkor a festéklézert pumpálja a megvilágító fényből az UV fényt kiszűrjük.
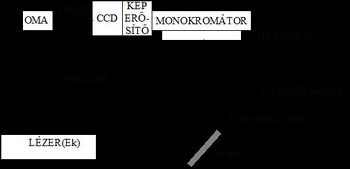
A felvillanó lézerfény a levélen széles hullámhossztartományban fluoreszcencia fény felvillanását eredményezi. A fluoreszcencia fényt egyrészt gyűjtőlencsével a monokromátor bemenő résére gyűjtjük, másrészt az élszűrővel megtisztítjuk a mintáról közvetlenül reflektált lézerfénytől. A monokromátor a fényt diszperziós rács segítségével felbontja, azaz a különböző hullámhosszúságú komponenseket különböző szög alatt diffraktálja. Ennek eredményeként a monokromátor képsíkjában a bemenő résen áthaladó fénykomponensek hullámhossz szerint térben kiterítve képződnek le. A képet egy CCD detektorral detektáljuk, melyben az egyes detektorelemek különböző hullámhosszúságú fényt látnak. Mivel a detektálandó fény spektrális intenzitása kicsi, a detektor előtt képerősítőt alkalmazunk. A képerősítő csak a villanás ideje alatt aktív, így a detektorra csak a villanás ideje alatt 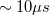 jut fény. Az optikai sokcsatornás analizátor (Optical Multichannel Analyzer = OMA) pedig az egyes detektor elemeken a villanások során észlelt fluoreszcencia fényt külön-külön tárolja és összegzi, majd kijelzi.
jut fény. Az optikai sokcsatornás analizátor (Optical Multichannel Analyzer = OMA) pedig az egyes detektor elemeken a villanások során észlelt fluoreszcencia fényt külön-külön tárolja és összegzi, majd kijelzi.
A továbbiakban a fontosabb alkotó elemek működését tekintjük át.
Az alkalmazott lézerek
A mérési feladatoknál a növények gerjesztése egyrészt nitrogén (N2) lézerrel, másrészt nitrogén lézerrel pumpált festéklézer segítségével történik. Ennek a fejezetnek az a célja, hogy a nitrogén-, illetve festéklézernél fellépő fizikai folyamatokat, illetve a lézer felépítését és jellemzőit röviden bemutassa.
A két gerjesztés közötti legfontosabb különbség, hogy amíg a nitrogén lézer egy önállóan működő ultraibolya lézer, addig a festéklézer gerjesztéséhez a nitrogénlézer szükséges. A festéklézeres mérésnél mindkét lézert alkalmazzuk.
N2 lézer[5]
A nitrogén lézer a gázlézerek közé tartozik. A gázok energiaszintjeinek kiszélesedése jóval kisebb, mint a szilárd testekéi. A gázokat általában alacsony nyomáson használják, így az ütközés miatti kiszélesedés kicsi, és a vonalszélességet a Doppler kiszélesedés határozza meg. Ezért a gáz lézereket általában elektromos úton gerjesztik, nagy áram átvezetésével. (A kis vonalszélesség miatt a lámpával történő pumpálás ez esetben jó hatásfokkal nem alkalmazható, hiszen bár a lámpák emissziós spektruma többé-kevésbé folytonos, a gázlézereknél nincs elég széles abszorpciós sáv az aktív anyagnál.) A populáció inverzió létrehozásához a gázlézereknél a következő követelményeknek kell teljesülnie:
- 1.) A magasabb lézernívóknak gerjesztése nagyobb, mint az alacsonyabbaké.
- 2.) A felső szint bomlásának lassabbnak kell lennie az alsónál.
Az utóbbi a folytonos üzemű működés szükséges feltétele. Amennyiben ez a feltétel nem teljesül, úgy a lézerműködés csak impulzus üzemben lehetséges, feltéve, hogy az első feltétel teljesül (ön-megszüntető lézer).
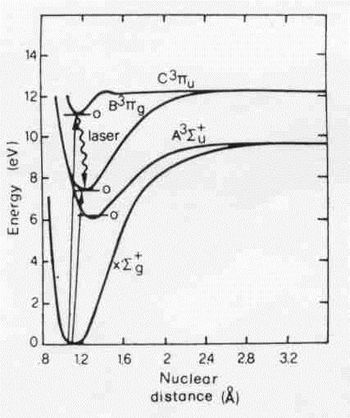
Az N2 lézer legfontosabb oszcillációja 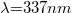 -nél van, ami az elektromágneses spektrum ultraibolya tartományában van, tehát nem látható! Ez a lézer az ön-megszüntető kategóriába tartozik. A N2 molekula energiaállapotait a következő grafikon szemlélteti:
-nél van, ami az elektromágneses spektrum ultraibolya tartományában van, tehát nem látható! Ez a lézer az ön-megszüntető kategóriába tartozik. A N2 molekula energiaállapotait a következő grafikon szemlélteti:
A lézerműködés a 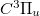 és a
és a 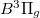 állapotok közötti átmenetnél áll fent. Mivel a C, és a B állapotok triplettek, így az átmenet az alapállapot felé első rendben kvantummechanikailag tiltott. Ennek megfelelően a B állapot élettartama hosszú (
állapotok közötti átmenetnél áll fent. Mivel a C, és a B állapotok triplettek, így az átmenet az alapállapot felé első rendben kvantummechanikailag tiltott. Ennek megfelelően a B állapot élettartama hosszú (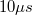 ), míg a C állapot sugárzási élettartama ennél rövidebb (40ns). Ez alapján látható, hogy a lézer folytonos üzemelésének feltétele nincs kielégítve. Lehetséges azonban 40 ns-nál rövidebb elektromos impulzusok segítségével gerjeszteni.
), míg a C állapot sugárzási élettartama ennél rövidebb (40ns). Ez alapján látható, hogy a lézer folytonos üzemelésének feltétele nincs kielégítve. Lehetséges azonban 40 ns-nál rövidebb elektromos impulzusok segítségével gerjeszteni.
A gyakorlatban 5-10ns-os gyors, kisülő impulzusokat alkalmaznak. Az impulzusok maximum 100Hz-es ismétlődési frekvenciával érkezhetnek, ezt a kisülő cső hűtése korlátozza.
Egy nitrogén lézer jellemző adatai (A mi lézerünk ettől valamelyest eltérhet.):
![\[ \begin{array}{|c c|} \hline L\acute{e}zerakt\acute{i}v\ anyag: & Nitrog\acute{e}n \\ Emisszi\acute{o}s\ hull\acute{a}mhossz: & 337\ nm \\ Ism\acute{e}tl\ddot{o}d\acute{e}si\ frekvencia: & 0-50 Hz \\ Nyal\acute{a}b\acute{a}tm\acute{e}r\ddot{o}: & 6\ mm \cdot 25\ mm\ (a\ kil\acute{e}p\acute{e}s\ hely\acute{e}n\acute{e}l)\\ Impulzusenergia: & 2,5\ mJ \\ Impulzus\ hossz: & 10\ ns \\ Impulzus\ cs\acute{u}csteljes\acute{i}tm\acute{e}ny: & 250\ kW \\ \hline \end{array} \]](/images/math/4/5/1/4519b5d3f859dc1e37a3920a7aeb947e.png)
Festéklézer[5]
A festéklézer lézeraktív anyaga folyadék halmazállapotú. Az oldott anyag szerves, az oldószer több fajta anyag lehet, például etil-alkohol, metil-alkohol, víz, … stb. A szerves festékeknek általában erős abszorpciós sávjai vannak az ultraibolya, és a látható tartományban. Ha ezen a megfelelő hullámhosszon gerjesztjük, akkor intenzív, széles sávú fluoreszcens sugárzást bocsátanak ki.
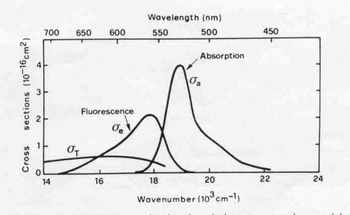
Az ábrán az abszorpciós, az emissziós, és a triplett-triplett átmenet spektrumjait láthatjuk a Rhodamine 6G festék esetében:
A 7. ábra jellegének megértése érdekében a festék molekulák energianívóit kell figyelembe vennünk. A továbbiakban az un. szabad elektron modellt írjuk le a cyanine festék esetében.
Az elektromos állapot a 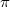 -elektronoktól származik, amiket modellezhetjük úgy, hogy szabadon mozoghatnak a molekula síkjában, amit két oldalról egy potenciál gát határol. Ennek megfelelően, legegyszerűbb közelítésként a következő energia szintekhez juthatunk:
-elektronoktól származik, amiket modellezhetjük úgy, hogy szabadon mozoghatnak a molekula síkjában, amit két oldalról egy potenciál gát határol. Ennek megfelelően, legegyszerűbb közelítésként a következő energia szintekhez juthatunk:
![\[E_n=\frac{h^2\cdot n^2}{8\cdot m\cdot L^2}\]](/images/math/b/4/a/b4ad78ffc5bb2dca13dd28657c1b727f.png)
ahol n egész szám, m az elektron tömege, L a potenciál völgy hossza.
A festék molekuláknak páros számú elektronja van a 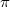 -felhőben. Ha 2N elektront tételezünk fel, akkor a legalacsonyabb energiaállapot az jelenti, hogy az elektronok megszállják a legalsó N energiaszintet, ahol minden szinten két elektron van, ellentétes spinekkel. Ehhez a molekulaállapothoz nulla összspin tartozik (szingulett állapot, S0).
-felhőben. Ha 2N elektront tételezünk fel, akkor a legalacsonyabb energiaállapot az jelenti, hogy az elektronok megszállják a legalsó N energiaszintet, ahol minden szinten két elektron van, ellentétes spinekkel. Ehhez a molekulaállapothoz nulla összspin tartozik (szingulett állapot, S0).
Az első gerjesztett szingulett állapot azt jelenti, hogy felgerjesztjük az egyiket a legmagasabb energiaállapotban levő elektronokból spin megfordítás nélkül magasabb energiájú állapotba (S1).
Ha a spin megfordul, akkor tripplett állapotról beszélünk (teljes spin = 1, T1). Ha az elektron eggyel még magasabb energiaállapotokba jut, akkor beszélünk S2, T2 állapotokról, és így tovább.
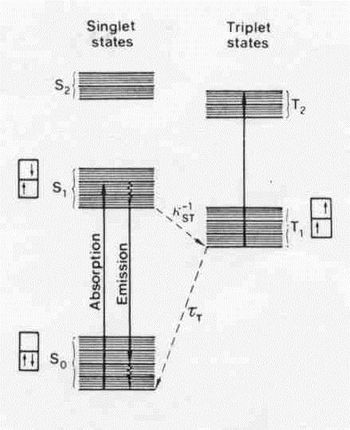
Az energiaállapotokat a következő grafikon szemlélteti:
Az egyes energiaállapotok a vibrációs szintekhez, illetve a rotációs szintekhez rendelhetőek. Mivel a sávkiszélesedés mechanizmusa a folyadékoknak jóval nagyobb, mint a szilárd anyagokénak, így a rotációs vonalak nincsenek felbontva, és a spektrum gyakorlatilag folytonossá válik.
Vizsgáljuk meg, hogy mi történik, ha a molekula elektromágneses sugárzás alá esik. A kiválasztási szabály megköveteli, hogy 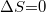 legyen. A szingulett-szingulett átmenet megengedett, csakhogy a szingulett-triplett átmenet tiltott. Emiatt az elektromágneses kölcsönhatás az elektronokat az alapállapotból (S0) egy S1 állapotába jutatja. Mivel a rotációs, és a vibrációs pályák folytonosak, így az abszorpciós spektrum széles, és folytonos a 7. ábra abszorpciós spektrumának megfelelően. A festékek érdekes tulajdonsága, hogy nagyon nagy a dipól mátrixeleme (
legyen. A szingulett-szingulett átmenet megengedett, csakhogy a szingulett-triplett átmenet tiltott. Emiatt az elektromágneses kölcsönhatás az elektronokat az alapállapotból (S0) egy S1 állapotába jutatja. Mivel a rotációs, és a vibrációs pályák folytonosak, így az abszorpciós spektrum széles, és folytonos a 7. ábra abszorpciós spektrumának megfelelően. A festékek érdekes tulajdonsága, hogy nagyon nagy a dipól mátrixeleme (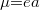 ), mivel a π-elektronok szabadon mozoghatnak a molekula dimenziójának nagyságrendjében (L). Így az abszorpciós hatáskeresztmetszet szintén nagy (
), mivel a π-elektronok szabadon mozoghatnak a molekula dimenziójának nagyságrendjében (L). Így az abszorpciós hatáskeresztmetszet szintén nagy (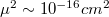 ).
).
A gerjesztett molekula állapot rögtön elbomlik az S1 szint legalacsonyabb vibrációs állapotába. Innen sugárzásos úton jut S0 néhány magasabb vibrációs állapotába (fluoreszcencia). (Az átmenet nagy valószínűséggel nem az alapállapotba történik, hanem a vibrációval gerjesztett állapotok valamelyikébe, az S0 sáv valamelyik felső nívójára!) A fluoreszcens emisszió így szintén egy széles, és folytonos hullámhossz tartományban jelentkezik, az abszorpciós sávnál nagyobb hullámhosszon, és kisebb frekvencián/energián, amint azt a 9. ábrán láthatjuk. Mivel a dipól mátrixelem nagy, így a stimulált emissziós hatáskeresztmetszet is nagy! Az alapállapot vibrációs-rotációs gerjesztett szintjei ezt követően nagyon rövid idő alatt (~10-13s) nem sugárzásos úton visszatérnek a legalacsonyabb vibrációs szintre.
Meg kell azonban jegyezni, hogy habár az 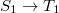 átmenet tiltott, az S1 állapot legalacsonyabb szintjéről az elektron T1 állapotba is kerülhet, ütközés útján. Hasonlóan
átmenet tiltott, az S1 állapot legalacsonyabb szintjéről az elektron T1 állapotba is kerülhet, ütközés útján. Hasonlóan 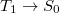 átmenet is nagyrészt ütközés miatt jön létre, de részben sugárzásos úton is (habár ez az átmenet első rendben szintén tiltott). Ezt a sugárzást nevezik foszforeszkálásnak. Itt jegyezzük meg, hogy a legalacsonyabb T1 energiaszint szintén abszorbeálhat sugárzást, ami
átmenet is nagyrészt ütközés miatt jön létre, de részben sugárzásos úton is (habár ez az átmenet első rendben szintén tiltott). Ezt a sugárzást nevezik foszforeszkálásnak. Itt jegyezzük meg, hogy a legalacsonyabb T1 energiaszint szintén abszorbeálhat sugárzást, ami 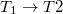 átmenetet eredményez, ami kvantummechanikailag megengedett!
átmenetet eredményez, ami kvantummechanikailag megengedett!
A lézerműködést lehetővé teszi, hogy gyors nemsugárzási átmenettel a gerjesztett S1 szingulett populáció nagyon gyorsan lejut a legalsó szintre, mialatt a gyors nem sugárzásos átmenet az alapállapoton belül a lézerátmenet alsó nívóját folyamatosan üríti. A mechanizmussal azonban több probléma van. Az első problémát az jelenti, hogy az S1 állapot élettartama nagyon rövid, ami nagy pumpálási energiát követelne meg. Szerencsére azonban a stimulált emissziós hatáskeresztmetszet is nagy, ami kompenzálja ezt a problémát. A második problémát a szingulett-triplett átmenet növekedése jelenti (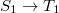 ). A
). A 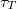 nagy a
nagy a 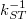 -vel összehasonlítva, így a molekulák felhalmozódnak a T1 állapotban. (
-vel összehasonlítva, így a molekulák felhalmozódnak a T1 állapotban. (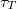 a T1 szint élettartama, kST a szingulett-triplett átmenet aránya, dimenziója s-1.) Ez jelentős abszorpciót eredményez a
a T1 szint élettartama, kST a szingulett-triplett átmenet aránya, dimenziója s-1.) Ez jelentős abszorpciót eredményez a 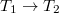 átmenetben. Sajnos ez az abszorpció általában ugyanabban a hullámhossz tartományban jelentkezik, mint a fluoreszcencia, emiatt súlyosan akadályozza a lézerműködést. Emiatt a folytonos lézer működés csak ritkán lehetséges, szükséges feltétele:
átmenetben. Sajnos ez az abszorpció általában ugyanabban a hullámhossz tartományban jelentkezik, mint a fluoreszcencia, emiatt súlyosan akadályozza a lézerműködést. Emiatt a folytonos lézer működés csak ritkán lehetséges, szükséges feltétele: 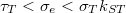 ,ahol
,ahol 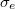 a stimulált emissziós hatáskeresztmetszet,
a stimulált emissziós hatáskeresztmetszet, 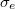 a triplett-triplett átmenet hatáskeresztmetszete. Impulzus üzemmódú működés azonban könnyebben elérhető, ennek feltétele, hogy a pumpáló impulzus időtartamának elegendően rövidnek kell lennie ahhoz, hogy túl nagy populáció ne halmozódjon fel a triplett állapotban. A harmadik fontos probléma az, hogy a pumpálás miatt hőmérséklet gradiens alakulhat ki a folyadékban, és ez hajlamos törésmutató gradiens létrehozására, ami akadályozza a lézerműködést.
a triplett-triplett átmenet hatáskeresztmetszete. Impulzus üzemmódú működés azonban könnyebben elérhető, ennek feltétele, hogy a pumpáló impulzus időtartamának elegendően rövidnek kell lennie ahhoz, hogy túl nagy populáció ne halmozódjon fel a triplett állapotban. A harmadik fontos probléma az, hogy a pumpálás miatt hőmérséklet gradiens alakulhat ki a folyadékban, és ez hajlamos törésmutató gradiens létrehozására, ami akadályozza a lézerműködést.
Az impulzus üzemű működést többféleképpen pumpálhatjuk: (1) gyors villanólámpával (a villanás időtartama<1µs); vagy (2) rövid fényimpulzus egy másik lézertől. Mindkét esetnél a rövid impulzus időtartam célja az, hogy lézer működést hozzon létre mielőtt észrevehető populáció halmozódik fel a triplett állapotban, és mielőtt törésmutató gradiens alakulna ki a folyadékban (az előbb felvetett két probléma). A lézeres pumpálások közül nagyon elterjedt a nitrogén lézeres pumpálás, hiszen ez egy UV lézer, ami alkalmas a legtöbb olyan festék pumpálására, amelyiknél az oszcilláció a látható tartományba esik. A pumpálás esetünkben is nitrogénlézerrel történik.
Nagyobb kisugárzási energia elérése érdekében a hatásosabb excimer lézerek (általában KrF, és XeF) elterjedőben vannak, ezek szintén UV lézerek. Az 550-600 nm -nél nagyobb emissziós hullámhosszú festékeknél a Q-kapcsolt másodharmonikus Nd:YAG lézer (λ = 532nm) a pumpáló. Ezeknek a látható pumpáló lézereknek a konverziós hatásfoka jóval nagyobb, mint amit UV lézeres pumpálással nyerhetünk, ráadásul a festékmolekulák roncsolódása is lényegesen kisebb.
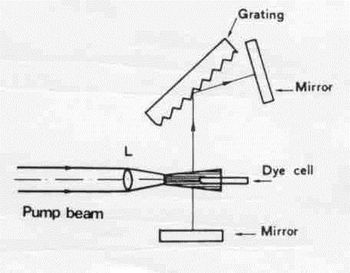
A mérési elrendezést tekintve az impulzus üzemben általában a transzverzális konfiguráció terjedt el:
A rács feladata az, hogy a széles emissziós sávból a rács forgatásával egy hullámhosszú lézerműködést tegyünk lehetővé.
Folytonos lézeres pumpáláshoz az Ar+ (illetve néha a Kr+) lézert használják. Ahhoz, hogy jóval kisebb lézerküszöböt érjünk el a CW pumpálásához longitudinális pumpálási konfigurációt használnak.
Egy festéklézer jellemző adatai (A mi lézerünk ettől valamelyest eltérhet.):
- Lézeraktív anyag: Lézerfesték
- Emissziós hullámhossz: 360 nm – 950 nm (a használt festékanyagtól függ)
- Ismétlődési frekvencia: 0-50Hz (a festéklézertől függ)
- Nyalábátmérő: 0,5 mm (a kilépés helyénél)
- Divergencia: 0,5 mrad
- Impulzusenergia: 0,3 mJ (Cumarin 2 festékkel 440 nm-nél)
- Impulzus hossz: 6 ns
Detektor
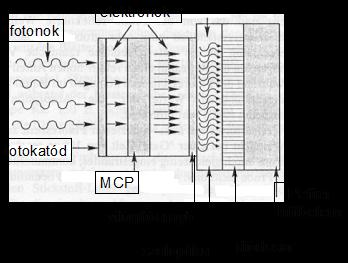
Mérési összeállításunkban detektorként egy termikusan stabilizált képerősítővel („image intesifier”) ellátott, 512 elemből álló szilícium fotodiódasor regisztrálja a térben hullámhossz szerint szétterített spektrumot. A képerősítő mikrocsatornalemez („microchannelplate”MCP) típusú. Az erősítőben a detektálandó fotonok egy fotokatódba ütköznek, ahonnan elektronokat löknek ki. Az elektronok a katódból kilépve jutnak a pár mikron átmérőjű, közvetlen egymás mellett elhelyezett mikrocsatornák közül abba, amelyik pont a fotonbecsapódás (elektronkiszabadulás) helyén van. A csatornán haladó elektron a gyorsító feszültség hatása alatt többször ütközik a csatorna falával, ahonnan szekunder elektronokat vált ki, és ezek szintén az anód irányába gyorsulnak, ütköznek. Ezáltal számuk megsokszorozódik és kilépve a csatornából egy világítóernyőbe csapódnak. Mivel a csatornák rendezetten, sűrűn egymás mellett helyezkednek el, így a beeső fotonok térbeli eloszlását képezik a világítóernyőre, csak nagyobb intenzitással. A világítóernyőn kialakuló, erősített képet száloptika képezi a fotodióda sorra. A diódasor elemeit az OMA szukcesszíven olvassa ki. A legkisebb képintegrálási idő (maximális időfelbontás 8.4 ms) A képerősítő triggerelhető, azaz az elektronokat gyorsító nagyfeszültséget digitálisan lehet be– és kikapcsolni. Ez teszi lehetővé a 3.1. pontban ismertetett triggerelt üzemmódot.
Jelfeldolgozás Optikai Sokcsatornás Analizátorral (OMA-val)
Az eddigiekben megismerkedtünk a gerjesztő fényforrással (nitrogén, illetve festéklézer), illetve a detektorral. Ebben a fejezetben a mérés jelfeldolgozó, és vezérlő egységével az optikai sokcsatornás analizátorral ismerkedhetünk meg.
Az optikai sokcsatornás analizátor alapvetően két üzemmódban dolgozhat. Egyrészt folytonos üzemmódban a detektorra érkező fényt a beállított mérési idő alatt mérheti. Másrészt lehetőségünk nyílik arra, hogy a detektálás időtartamát egy külső, vagy egy belső trigger jel segítségével határozzuk meg. Mivel a fluoreszcens jelek a háttérfényhez képest kicsik, így nekünk ezt a módszert kell alkalmaznunk, és a fényt csak a fluoreszkálás ideje alatt detektáljuk.
A hallgatói mérésnél az OMA belső szinkronjelét használjuk. A mérésnél az OMA a beállított gyakorisággal 12 s hosszú négyszög jelet küld, ezt mi 2 részre osztjuk. A jel egyrészt egy impulzus erősítő után a detektorra jut, ami ezt követően – ha GATE üzemmódba állítjuk – akkor csak az impulzus ideje alatt lesz nyitva. Másrészt a jel a nitrogén lézerre jut, és külső trigger jelként alkalmazzuk. Mivel a beérkező impulzus és a lézer impulzus között az időkülönbség mindössze 0.6-1.0 s, a detektor áramköre pedig még gyorsabb, így a lézer villanásának ideje alatt (~ 10 ns) a detektor nyitva van, tehát a fluoreszcens fényt detektáljuk.
Az OMA-val beállíthatjuk azt is, hogy egy mérésnél hány impulzust összegét akarjuk detektálni, illetve hány ilyen méréssorozatot akarunk mérni. Ez a funkció a méréseink kiértékelését teszi könnyebbé. Emellett lehetőség van arra, hogy csak minden n-dik impulzust detektáljuk, ezt a funkciót azonban ebben a hallgatói mérésben nem használjuk ki.
Mérési feladatok
Eszközök kezelése
A mérés kezdetekor kapcsoljuk fel a két főkapcsolót, és kapcsoljuk be a nitrogén lézert a kulcs ¼-del óramutató járásának megfelelő irányú elfordításával. Ezt követően körülbelül 15 percet kell várnunk arra, hogy a THYRATRON FILAMENT hűtése megkezdődjön. A lézert akkor lehet indítani, ha a TIME DELAY lámpa elalszik.
Amikor a TIME DELAY lámpa kialszik, akkor indítsuk be a vákuum szivattyút, és a nyomás a kisülő csőben lecsökken. Ezt követően megnyitjuk a Nitrogén gázpalackot a gázpalacknál, majd a lézernél olyan módon, hogy a PRESSURE ADJUST kapcsolót megnyitjuk (open állás). Ezt követően a gázpalacknál 1,5 bar kilépő nyomást kell tapasztalnunk. (Ha más nyomást észlelünk, akkor állítsuk 1,5 bar-ra!) A kisülő csőben pedig 40-60 torr nyomásnak kell lennie. (Ha más nyomást észlelünk, akkor állítsuk be ebbe a tartományba a mellette levő nyomás beállító segítségével.)
Ha minden a megfelelő állapotba került, akkor egyetlen lámpa sem világít, és a lézert a START gomb folyamatos nyomásával indíthatjuk. Ezt követően az impulzusok ismétlődési frekvenciáját a REPETITION RATE gombbal beállíthatjuk, változtathatjuk. A lézer lekapcsolása a STOP gomb megnyomásával történik. Ha a kulcsot nem fordítjuk el, akkor a lézer a START gomb megnyomásával azonnal újraindítható.
Ezt követően indítsuk be az OMA-t. Ehhez először a feszültségstabilizátort kell bekapcsolnunk, majd magát az OMA-t. A bejövő ablak érintőgombos felületén válasszuk a MAIN MENU-t. Ezt követően 12 menü pontból választhatunk, amelyek közül a mérésünkhöz az DATA ACQUISITION és a DISK OPERATING SYSTEM menü pontokra lesz szükségünk. Válasszuk a DATA ACQUISITION menü pontot, itt történik a mérés beállítása. Válasszuk az EXPTIME (msec) menü pontot, és állítsunk be 200 msec/scan mérési időt! (Illetve később ez impulzus ismétlődési frekvenciát fog jelenteni, miután az OMA-t folytonos üzemmódból impulzus üzemmódba állítottuk!)
Az impulzus üzemmódba való átállításhoz a D.A. MD MENU menü pontot válasszuk. Itt a LIVE NO TRIG gomb (második sor utolsó) TRIGGER-re állításával elértük azt, hogy a mérésünk az OMA trigger jelére indul, és végződik (impulzus üzemmód). A D.A. MD MENU menüpontban történik a mérés beállítása is. A SCANS I gombbal adhatjuk meg, hogy egy mérésnél hány impulzust mérjünk, a MEM’S J gombbal adhatjuk meg a méréssorozatok számát. Az IGNORES K gombbal adjuk meg, hogy minden hány impulzust hagyjon ki a műszer, ez a mérés során mindvégig 0-án maradjon! Miután a mérést beállítottuk menjünk vissza a DATA ACQUISITION menü pontba a RETURN gomb segítségével. Itt a LIVE gomb kétszeri megnyomásával állítsuk be az ACCUM. üzemmódba, melynek hatására mérési eredményeinket később fájlba konvertálhatjuk!
Ezt követően állítsuk a nitrogén lézert külső trigger jeles üzemmódba. Ezt a REPETITION RATE gomb óramutató járásával ellentétes irányba végállásig (kattanás után) való forgatásával érhetjük el. Ezt követően a lézerünk az impulzusokat az OMA trigger jelének megfelelően szolgáltatja, ha a START gombbal elindítjuk. (Ne használjunk a 200 msec/scan-nál lényegesen gyakoribb impulzusokat, mert ennél gyakoribb impulzusok szolgáltatására lézerünk nem alkalmas!)
A mérési eredményeket az OMA speciális úgynevezett OMA fájlokban tárolja. Ezeket a DISK OPERATING SYSTEM menü pontban konvertálhatjuk át DOS fájlba. A legegyszerűbb, ha ezt mindjárt a mérést követően megtesszük, hiszen nekünk az OMA fájlokra nincs szükségünk. Ezért a mérés után tegyünk az alsó (1-es) meghajtóba egy DOS formázott lemezt. Ezt követően válasszuk az OMAMS-DOS menü pontot. Itt válasszuk az ACCUM. menü pontot, hiszen a mérési eredményt közvetlenül átalakítjuk. Ezt követően a program megkérdezi, hogy hányadiktól hányadikig indexelt méréssorozatokat akarjuk kimenteni. Ezután már csak a cél fájlt kell megadni (például: 1:meres.san).
Mérés menete
A végzett mérés két részből áll, egyrészt méréseket végzünk nitrogén lézerrel, másrészt nitrogénnel pumpált festéklézerrel.
Először a mérést a nitrogénlézerrel végezzük. A MÉRÉS SORÁN HASZNÁLJUNK UV-VÉDŐ SZEMÜVEGET! Egy papírlap segítségével azonosítsuk a lézernyalábot. (A papír lézer hatására fluoreszkál, így a nyaláb helye láthatóvá válik.) Pozícionáljuk a lézert a mintatartóban elhelyezett levélre. Használjunk egy körülbelül 6 cm fókusztávolságú lencsét, és a kétszeres fókuszból képezzük le a kétszeres fókuszba a fluoreszcens fényt. A fluoreszkálás kiindulási helye a mintatartó azon pontja, ahová az UV fény érkezik. A helyes beállításhoz használjunk egy kis méretű ragasztó papírt, ezt a levélre ragasszuk, mivel ez nagyon erősen fluoreszkál, így nagy jelhez juthatunk. A beállítást célszerű folytonos üzemmódban végezni, így az OMA-t folyamatos üzemmódra állítsuk, és a lézer belső triggerelést válasszunk. A beállításnál figyeljünk arra, hogy a papírról érkező fény ne vigye telítésbe a detektort, ezt elkerülendő a papír méretét, ha kell, akkor csökkentsük. Miután a beállítás megtörtént, a ragasztó papírt távolítsuk el. Az 1. Mérési feladatot ezután elvégezhetjük.
A második mérés előtti átalakítás előtt a NITROGÉNLÉZERT ÁLLÍTSUK LE! Csatlakoztassuk a festéklézert a nitrogénlézerhez. Figyeljünk arra, hogy a festék lézer oldallapja párhuzamos legyen a nitrogénlézer oldallapjával! Nyissuk fel a festéklézer előlapját! A küvettát az előre elkészített 7D4MC festékkel tegyük a küvetta tartóba! Állítsuk be a rács számlálóját 27600-as állásba! (Ekkor a lézerünk – ennél a festéknél – 6-dik rendben 460nm-en fog működni.) Indítsuk el a nitrogén lézert, és a kilépés előtt egy papírlappal figyeljük a lézernyaláb alakját. Középen egy fényes körben lényegesen nagyobb intenzitást kell tapasztalnunk. Ha nem így van, és nincs erős intenzitású folt(ok), akkor forgassuk el a küvettát 90º-kal! Ha egy pontnál több van akkor a fedőlapon levő két pozícionálókat tekerjük addig, amíg a lehető legjobban egy pontba nem tudjuk koncentrálni a meglevő fényintenzitást. Ezt követően a lézer kilépő apertúrát a lehető legjobban nyissuk ki, a lézer tetejét csukjuk le! Az előzőhöz hasonlóan itt is a kétszeres fókuszból a kétszeres fókuszba képezzük le a fluoreszcens fényt! A beállításnál segítségünkre lehet a direkt reflektált lézerfény, a leképezést ennek segítségével optimalizáljuk. A beállítást ebben az esetben is folytonos üzemmód mellett célszerű elvégezni. A kilépő lézer apertúráját a külső rekesszel mindig csökkentsük le annyira, hogy a detektor ne menjen telítésbe! Miután az elérhető optimális beállítást megtaláltuk, helyezzük be a 630nm-es felül áteresztő szűrőt a detektor elé. (Így kiküszöbölhetjük a direkt visszavert lézerfény a fluoreszcens fényhez képest nagy intenzitását.) Nyissuk ki maximálisra a lézer kilépő apertúráját, és elvégezhetjük a 2. Mérési feladatot.
Mérési feladatok
1.) Növényi fluoreszcencia kinetikájának vizsgálatok UV lézerrel
A feladat a mérési elrendezés összeállítása. Ezt követően előbb mérjük meg a hátteret, ami szinte kizárólag elektromos zajból származik. Válasszunk azt, hogy az impulzusok 0,2 másodpercenként kövessék egymást (200msec/scan)! Mérjünk egy mérés sorozatot 5 impulzussal (SCANS I = 5, MEM’S J=1, IGNORES K = 0)! Indítsuk be a lézert, külső triggeléses üzemmódban, és mérjük a fluoreszcenciát! Mérjünk 20 sorozatot, sorozatonként 5 impulzussal! (SCANS I = 5, MEM’S J=20, IGNORES K = 0) Hasonlítsuk össze az egyes háttérrel korrigált méréseket! Milyen hullámhosszakon van fluoreszcencia csúcsa? A különböző időpontokban végzett méréseket összehasonlítva, mit tudunk mondani a fluoreszcencia időbeli változásáról? Tudunk-e valamilyen heurisztikus magyarázatot adni fluoreszcencia kinetikájára?
2.) Klorofill fluoreszcencia vizsgálatok festéklézerrel
Ebben az esetben is állítsuk össze a korábban említett mérési elrendezést. Először ebben az esetben is a hátteret mérjük le, alkalmazzuk az előző mérésben is alkalmazott impulzus gyakoriságot. Mérjünk egy mérés sorozatot 10 impulzussal (SCANS I = 10, MEM’S J=1, IGNORES K = 0)! )! Indítsuk be a lézert, külső triggeléses üzemmódban, és mérjük a fluoreszcenciát! Mérjünk 20 sorozatot, sorozatonként 10 impulzussal! (SCANS I = 10, MEM’S J=20, IGNORES K = 0) A mérésidő körülbelül felénél (10*10*0,2/2 =10 sec) kapcsoljunk be egy asztali lámpát, amelynek fényét közvetlenül a levélre irányítottunk! (A levélre sok fény jusson!) Értékeljük ki a méréseinket! Hol vannak a fluoreszcencia csúcsai? Melyik mérés sorozatnál kapcsoltuk be a lámpát, mi a lámpa bekapcsolásának hatása?
Elgondolkodtató kérdések
A következő kérdések megválaszolása a mérési elrendezés, illetve a mérés jobb megértését teszi lehetővé. http://fizipedia.phy.bme.hu/skins/common/images/button_italic.png 1.) A nitrogénlézerhez egy nitrogén eltávolítása érdekében egy vákuum szivattyút csatlakoztatunk. Mi a legfontosabb szempont a szivattyú ki választásakor? A nagy végvákuum?
2.) Az UV gerjesztésnél a levél láthatóan kék színben fluoreszkál. Mi mégis a spektrum piros tartományban mérünk nagyobb fluoreszcenciát. Miért?
3.) A levek abszorpciós maximuma 440nm körül van, és az abszorpció 460nm-en nagyobb, mint 337nm-en. Mégis az UV gerjesztésnél mérünk nagyobb fluoreszcenciát. Miért?
4.) Ha a levél abszorpciós maximuma 440 nm-en van, akkor a hangolható festéklézerünkkel miért nem kisebb hullámhosszon mérünk?
Javasolt irodalom
- Stober F., Untersuchungen zur Laser-induzierten Blau-,Grün- und Rotfluoreszenz an Pflanzen unter Einsazt eines optischen Vielkanalanalysators (OMA). Doktori értekezés, University of Karlsruhe, 1993
- Kautsky H., Hirsch A., Neue Versuche zur Kohlensäureassimilation. Die Naturwissenschaften 19, 964, 1931
- Kautsky H., Hirsch A., Chlorophyllfluoreszenz und Kohlensäureassimilation. I. Mitteilung: Das Fluoreszenzverhalten grüner Pflanzen. Biochemische Zeitschrift 247, 423-434, 1934
- Sorokin P., Lankard J. R. IBM J. Res. Develop. 10, 162, 1966
- Svelto O., Principles of Lasers, Plenum Press New York & London, 1998
PDF formátum
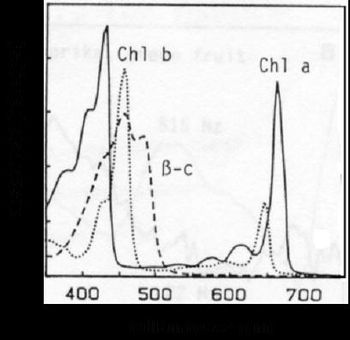
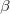 -karotenoid abszorpciós spektruma 2. ábra
-karotenoid abszorpciós spektruma 2. ábra