„Vékonyréteg leválasztás” változatai közötti eltérés
| 6. sor: | 6. sor: | ||
=== Fizikai elméleti alapok === | === Fizikai elméleti alapok === | ||
| − | |||
==== Egyensúlyi telített gőznyomás ==== | ==== Egyensúlyi telített gőznyomás ==== | ||
<wlatex> | <wlatex> | ||
A lap 2013. március 24., 13:30-kori változata
SZERKESZTÉS ALATT!!
Vákuumpárologtatás / vákuumgőzölés
A vákuumpárologtatás - vékonyrétegek előállítására szolgáló - fizikai gőzfázisú leválasztási eljárás (PVD, Physical Vapor Deposition). A leválasztani kívánt anyagot vákuumtérben - magas hőmérsékletre hevítve - elpárologtatják, majd az a bevonni kívánt munkadarab / hordozó / szubsztrát felületére lekondenzálva kialakítja a vékonyréteget.
Fizikai elméleti alapok
Egyensúlyi telített gőznyomás
Egy zárt rendszerben 0 K-nél magasabb, állandó T hőmérsékleten az anyag felületéről kilépő és a felületre visszatérő atomok dinamikus egyensúlyban vannak, melyet az adott hőmérséklethez tartozó P egyensúlyi telített gőznyomással (tenzióval) jellemezhetünk. Az egykomponensű rendszer két fázisának egyensúlyi feltételét a Clausius-Clapeyron egyenlet adja meg:
ahol 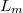 a fázisátalakuláshoz szükséges moláris hőmennyiség,
a fázisátalakuláshoz szükséges moláris hőmennyiség, 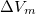 pedig a két fázis móltérfogatának különbsége
pedig a két fázis móltérfogatának különbsége 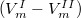 .
.
Szilárd-gőz fázisátalakulás esetén a szilárd fázis moláris térfogata 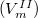 elhanyagolható a gőz fázis moláris térfogata
elhanyagolható a gőz fázis moláris térfogata 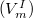 mellett, így a
mellett, így a 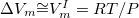 (R: az egyetemes gázállandó) összefüggést az Sablon:EquationNote egyenletbe behelyettesítve az alábbi összefüggést kapjuk:
(R: az egyetemes gázállandó) összefüggést az Sablon:EquationNote egyenletbe behelyettesítve az alábbi összefüggést kapjuk: