Termodinamika példák - Entrópiaváltozás izobár táguláskor
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. április 13., 21:59-kor történt szerkesztése után volt.
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Entrópia, II. főtétel |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Mennyivel változik meg
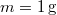 nitrogéngáz entrópiája, ha állandó nyomáson
nitrogéngáz entrópiája, ha állandó nyomáson 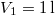 térfogatról
térfogatról 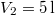 térfogatra expandáltatjuk.
térfogatra expandáltatjuk.
Megoldás
Az entrópiaváltozás definíciója
![\[ mathrm{d}S = \frac{\delta Q}{T}, \]](/images/math/4/1/5/41592112a8467d4865f2a744b00da8cc.png)
amibe helyettesítsük be a közölt hő első főtételből kifejezett
![\[ \delta Q = mathrm{d}U+p\,mathrm{d}V \]](/images/math/f/2/7/f2733cba6b296a581460567ffddfcec0.png)
alakját, ahol 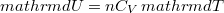 és
és 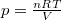 :
:
![\[ mathrm{d}S= n C_V \frac{mathrm{d}T}{T} + nR \frac{mathrm{d}V}{V}. \]](/images/math/4/b/d/4bdd7b4ac518ae1dc8be40b4fb0f1bbd.png)
Kiintegrálva az egyenletet 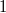 kezdeti- és
kezdeti- és 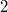 végállapot között:
végállapot között:
![\[ S_2 - S_1 = nR \ln\frac{T_2}{T_1} + nR \ln\frac{V_2}{V_1}, \]](/images/math/c/8/3/c83d63e7448ff9ba2f09138b5e4d15b6.png)
ahol most izotermikusan 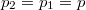 ezért
ezért 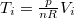 (
(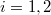 ):
):
![\[\]](/images/math/b/8/3/b83fa70287c65f9e336c48e0eb4ff152.png)