Termodinamika példák - Entrópiaváltozás egyensúlyig kaloriméterben
A Fizipedia wikiből
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Entrópia, II. főtétel |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
-
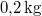 ,
, 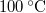 hőmérsékletű vasat hőszigetelt kaloriméterben lévő,
hőmérsékletű vasat hőszigetelt kaloriméterben lévő, 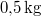 ,
, 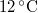 -os vízbe teszünk. A vas fajhője
-os vízbe teszünk. A vas fajhője 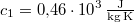 , a vízé
, a vízé 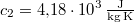 . Mennyi az entrópiaváltozás a hőmérséklet kiegyenlítődése miatt, ha a nyomás állandó?
. Mennyi az entrópiaváltozás a hőmérséklet kiegyenlítődése miatt, ha a nyomás állandó?
Megoldás
A közös 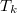 hőmérsékletet abból kapjuk meg, hogy a vas által leadott hő megegyezik a víz által felvett hővel:
hőmérsékletet abból kapjuk meg, hogy a vas által leadott hő megegyezik a víz által felvett hővel:
![\[ c_1 m_1\left(T_1-T_k\right) = c_2 m_2\left(T_k-T_2\right), \]](/images/math/0/2/9/02951c3781a3ec73663516e9f5623706.png)
ahol 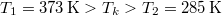 rendre a vas kezdeti, a közös és víz kezdeti hőmérséklete,
rendre a vas kezdeti, a közös és víz kezdeti hőmérséklete, 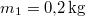 a vas,
a vas, 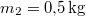 a víz tömege.
a víz tömege.
![\[ T_k = \frac{c_1 m_1 T_1+ c_2 m_2 T_2}{c_1 m_1+ c_2 m_2}\approx 288{,}7\,\mathrm{K}. \]](/images/math/9/9/c/99c652dc13378053792469df258c0a7f.png)
Az entrópiaváltozás a részrendszerek entrópiaváltozásának összege:
![\[ \Delta S = \int_{T_1}^{T_k} \frac{c_1 m_1} T\,\mathrm{d}T + \int_{T_2}^{T_k} \frac{c_2 m_2} T\,\mathrm{d}T = c_1 m_1 \ln\frac{T_k}{T_1} + c_2 m_2 \ln\frac{T_k}{T_2} \approx - 23{,}57 \mathrm{\frac{J}{K}} + 26{,}97 \mathrm{\frac{J}{K}} = 3{,}41 \mathrm{\frac{J}{K}}. \]](/images/math/7/a/2/7a20e7c08d2085589cd1932cca84299b.png)