„Termodinamika példák - Keveredési entrópia, Gibbs-paradoxon” változatai közötti eltérés
| 35. sor: | 35. sor: | ||
$$ \Delta S = R \left( n_1 \ln\frac{n_1+n_2}{n_1}+ n_2 \ln\frac{n_1+n_2}{n_2}\right)>0. $$ | $$ \Delta S = R \left( n_1 \ln\frac{n_1+n_2}{n_1}+ n_2 \ln\frac{n_1+n_2}{n_2}\right)>0. $$ | ||
| − | '''c)''' Ha a két edényben azonos gáz van, akkor bármelyik pillanatban munkavégzés nélkül visszatehetjük a válaszfalat és ugyanúgy az ''egyensúlyi'' kezdeti makroállapotot kapjuk eredményként, az entrópia nem változhatott meg noha a ''b)'' pontban kapott eredmény | + | '''c)''' Ha a két edényben azonos gáz van, akkor bármelyik pillanatban munkavégzés nélkül visszatehetjük a válaszfalat és ugyanúgy az ''egyensúlyi'' kezdeti makroállapotot kapjuk eredményként, az entrópia nem változhatott meg: |
| + | $$ \Delta S = 0, $$ | ||
| + | noha a ''b)'' pontban kapott eredmény az entrópia növekedését sugallná, ez a Gibbs-paradoxon. | ||
| − | |||
== Megjegyzés: a Gibbs-paradoxon == | == Megjegyzés: a Gibbs-paradoxon == | ||
Az eltérés a klasszikus részecskeképben és az entrópia definíciójában keresendő: a végállapot entrópiájának számításakor feltettük, hogy meg tudjuk különböztetni, kezdetben melyik részecske melyik tartályban volt, ami különböző anyagi minőség esetén lehetséges is. A kvantummechanika eredményei szerint viszont az azonos anyagi minőségű részecskék ''megkülönböztethetetlenek'', azaz miután egyetlen közös térbe engedtük őket, elméletben sincs olyan mérés, ami egyszerre megmondja a kezdőfeltételeket (a részecskék pontos sebességét ''és'' pontos helyét), sem olyan, amelyik megmondja, melyik részecske eredetileg melyik tartályban volt. | Az eltérés a klasszikus részecskeképben és az entrópia definíciójában keresendő: a végállapot entrópiájának számításakor feltettük, hogy meg tudjuk különböztetni, kezdetben melyik részecske melyik tartályban volt, ami különböző anyagi minőség esetén lehetséges is. A kvantummechanika eredményei szerint viszont az azonos anyagi minőségű részecskék ''megkülönböztethetetlenek'', azaz miután egyetlen közös térbe engedtük őket, elméletben sincs olyan mérés, ami egyszerre megmondja a kezdőfeltételeket (a részecskék pontos sebességét ''és'' pontos helyét), sem olyan, amelyik megmondja, melyik részecske eredetileg melyik tartályban volt. | ||
| + | |||
| + | A ''b)'' pontban kapott eredményt $N_\text{Av} n_j = N_j$ összefüggéessel átírjuk részecskeszámokra | ||
| + | $$ \Delta S = k \left( N_A \ln\frac{N_A+N_B}{N_1}+ N_B \ln\frac{N_A+n_B}{N_B}\right)>0, $$ | ||
| + | ahol $N_\text{Av}$ az Avogadro-, $k$ pedig a Boltzmann-állandó. | ||
| + | |||
| + | Tekintsük most az entrópia Boltzmann-féle definícióját: | ||
| + | $$ S = k \ln W, $$ | ||
| + | ahol $W$ a makroállapotot megvalósító lehetséges mikroállapotok száma. | ||
| + | A kezdeti állapotban a mikroállapotok száma a két edény mikroállapotai számának szorzata, hiszen a két edény egymástól független rendszer: | ||
| + | $$ W_\text{kezd} = W_1 \cdot W_2, $$ | ||
| + | a végállapotot jelölje $W_\text{vég}$, amikkel: | ||
| + | $$ \Delta S $$ | ||
| + | |||
| + | ... folyt ... | ||
Ezért az entrópiadefiníciót ki kell egészítenünk a megkülönböztethetetlenséggel, azaz azonos anyagi minőségű részecskék permutációja nem vezet új makroállapothoz: | Ezért az entrópiadefiníciót ki kell egészítenünk a megkülönböztethetetlenséggel, azaz azonos anyagi minőségű részecskék permutációja nem vezet új makroállapothoz: | ||
| 64. sor: | 79. sor: | ||
$$\Delta S=k\ln \frac{W_2}{W_1}=0.$$ | $$\Delta S=k\ln \frac{W_2}{W_1}=0.$$ | ||
| − | Ha kezdetben a két edényben különböző gázok volnának, akkor $ | + | Ha kezdetben a két edényben különböző gázok volnának, akkor $W'_1$-ben az $\frac{\left( N_1+ N_2\right)!}{N_1! N_2!}$ tényező eltűnne, hiszen csak egyféleképpen tudnánk szétosztani a részecskéket a tartályok között. Ekkor: |
$$\Delta S=k\ln \frac{W_2}{W_1}=k\ln \frac{\left( N_1+ N_2\right)!}{N_1! N_2!}.$$</small> | $$\Delta S=k\ln \frac{W_2}{W_1}=k\ln \frac{\left( N_1+ N_2\right)!}{N_1! N_2!}.$$</small> | ||
| − | Vegyük észre, hogy a fal felnyitása előtt és után ugyanannyi részecske volt az egyes képzeletbeli cellákban, ez csak egyensúlyban, makroszkopikusan nagy cellákra igaz. Vegyük még észre, hogy élhetünk a $p=q=1$ választással, ekkor azonos fajtájú gázra $W_1$ és $W_2$ már az egyszerűsítés előtt ugyanazt az alakot ölti, ami a gázrészecskék egymás közötti teljes felcserélhetőségére utal, ami a kezdőállapotban kvantummechanikailag nem is igaz; különböző fajtájú gázokra $ | + | Vegyük észre, hogy a fal felnyitása előtt és után ugyanannyi részecske volt az egyes képzeletbeli cellákban, ez csak egyensúlyban, makroszkopikusan nagy cellákra igaz. Vegyük még észre, hogy élhetünk a $p=q=1$ választással, ekkor azonos fajtájú gázra $W_1$ és $W_2$ már az egyszerűsítés előtt ugyanazt az alakot ölti, ami a gázrészecskék egymás közötti teljes felcserélhetőségére utal, ami a kezdőállapotban kvantummechanikailag nem is igaz; különböző fajtájú gázokra $W'_1=1$ és $W'_2=\frac{\left(N_1+ N_2\right)!}{N_1! N_2!}$, amit könnyebben magyarázhatunk a megkülönböztethetőséggel. |
</wlatex> | </wlatex> | ||
</noinclude> | </noinclude> | ||
A lap 2013. április 15., 21:52-kori változata
| Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Entrópia, II. főtétel |
Feladatok listája:
|
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Egymástól válaszfallal elzárt,
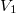 és
és 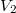 térfogatú két edényben azonos hőmérsékletű, azonos nyomású,
térfogatú két edényben azonos hőmérsékletű, azonos nyomású, 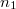 és
és 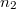 mólszámú, különböző fajtájú ideális gáz van. Ha a válaszfalat eltávolítjuk, akkor a két gáz összekeveredik.
mólszámú, különböző fajtájú ideális gáz van. Ha a válaszfalat eltávolítjuk, akkor a két gáz összekeveredik.
- a) Indokoljuk meg, hogy a folyamatban miért nem változik a hőmérséklet és a nyomás!
- b) Határozzuk meg az entrópia-változást (az ún. keverési entrópiát), és fejezzük ki a gázok
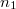 és
és 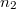 mólszámaival!
mólszámaival!
- c) Számítsuk ki az entrópia-változást, ha a két edényben azonos fajtájú gáz van!
Megoldás
a)A két edény paramétereit alsó indexek számokkal (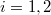 ), a gázokat betűkkel (
), a gázokat betűkkel (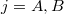 ) különböztetjük meg. Kezdetben az állapotegyenletek:
) különböztetjük meg. Kezdetben az állapotegyenletek:
![\[ p V_1= N_A kT, \qquad p V_2= N_B kT. \]](/images/math/7/1/6/7160b87e0f65b613d97a1d7be64dd0b0.png)
A fal elvétele után a Dalton-törvényt felhasználva a kialakuló parciális nyomások:
![\[ p_A=\frac{N_A kT} {V_1+ V_2}, \qquad p_B=\frac{N_B kT} {V_1+ V_2}\]](/images/math/8/a/2/8a23b638d6848dc10e68b20dc8b49881.png)
és a 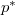 össznyomás
össznyomás
![\[ p^* = p_1+p_2 = \frac{N_A kT + N_B kT}{V_1+ V_2} = \frac{p V_1 + p V_2}{V_1+ V_2} = p. \]](/images/math/4/7/3/4730c8124db74341d7193acc1f52f02d.png)
b) Az I. főtételt kiintegrálva korábban megkaptuk az entrópia hőmérséklet- és térfogatfüggését:
![\[ \Delta S_j = n_j C_{Vj} \ln\frac{T_{j\text{vég}}}{T_{j\text{kezd}}} +n_j R \ln\frac{V_{j\text{vég}}}{V_{j\text{kezd}}}, \]](/images/math/b/0/f/b0f51b192980c16371c16c6dd60154f3.png)
most 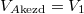 ,
, 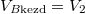 és
és 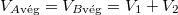 .
.
Most a hőmérséklet végig állandó (az a) részben azt láttuk be, hogy a kezdeti- és a végállapotban ugyanaz, a feladat megoldásához ez is elég). Ezekkel a két gáz entrópia-változásának összege:
![\[ \Delta S = k\left(N_A \ln\frac{V_1+V_2}{V_1}+ N_B\ln \frac{V_1+V_2}{V_2}\right) \]](/images/math/3/d/b/3db079045496ef23438e9ad9c6ab1bd8.png)
![\[ V_1=\frac{n_A RT} p, \qquad V_2=\frac{n_B RT} p\]](/images/math/5/a/a/5aa378fceca4cdffcb5ef5bef98dc9e9.png)
![\[ \Delta S = R \left( n_A \ln\frac{n_A+n_B}{n_1}+ n_B \ln\frac{n_A+n_B}{n_B}\right)>0, \]](/images/math/c/6/4/c64cbd8d19854abd0f89e455453b61b0.png)
ami a feladatban adott 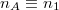 és
és 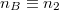 értékekkel
értékekkel
![\[ \Delta S = R \left( n_1 \ln\frac{n_1+n_2}{n_1}+ n_2 \ln\frac{n_1+n_2}{n_2}\right)>0. \]](/images/math/3/7/5/3755081c693f99bf4c4e41631fac60d8.png)
c) Ha a két edényben azonos gáz van, akkor bármelyik pillanatban munkavégzés nélkül visszatehetjük a válaszfalat és ugyanúgy az egyensúlyi kezdeti makroállapotot kapjuk eredményként, az entrópia nem változhatott meg:
![\[ \Delta S = 0, \]](/images/math/9/c/4/9c42fd9c23c5c5501663b1d6c7b963bb.png)
noha a b) pontban kapott eredmény az entrópia növekedését sugallná, ez a Gibbs-paradoxon.
Megjegyzés: a Gibbs-paradoxon
Az eltérés a klasszikus részecskeképben és az entrópia definíciójában keresendő: a végállapot entrópiájának számításakor feltettük, hogy meg tudjuk különböztetni, kezdetben melyik részecske melyik tartályban volt, ami különböző anyagi minőség esetén lehetséges is. A kvantummechanika eredményei szerint viszont az azonos anyagi minőségű részecskék megkülönböztethetetlenek, azaz miután egyetlen közös térbe engedtük őket, elméletben sincs olyan mérés, ami egyszerre megmondja a kezdőfeltételeket (a részecskék pontos sebességét és pontos helyét), sem olyan, amelyik megmondja, melyik részecske eredetileg melyik tartályban volt.
A b) pontban kapott eredményt 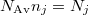 összefüggéessel átírjuk részecskeszámokra
összefüggéessel átírjuk részecskeszámokra
![\[ \Delta S = k \left( N_A \ln\frac{N_A+N_B}{N_1}+ N_B \ln\frac{N_A+n_B}{N_B}\right)>0, \]](/images/math/b/e/a/beaeefb07cb0edeb0e625a56a760573c.png)
ahol 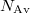 az Avogadro-,
az Avogadro-, 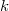 pedig a Boltzmann-állandó.
pedig a Boltzmann-állandó.
Tekintsük most az entrópia Boltzmann-féle definícióját:
![\[ S = k \ln W, \]](/images/math/e/8/c/e8c712fad5345992cd44310ac103ec0d.png)
ahol 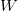 a makroállapotot megvalósító lehetséges mikroállapotok száma.
A kezdeti állapotban a mikroállapotok száma a két edény mikroállapotai számának szorzata, hiszen a két edény egymástól független rendszer:
a makroállapotot megvalósító lehetséges mikroállapotok száma.
A kezdeti állapotban a mikroállapotok száma a két edény mikroállapotai számának szorzata, hiszen a két edény egymástól független rendszer:
![\[ W_\text{kezd} = W_1 \cdot W_2, \]](/images/math/c/0/c/c0cd8a6abc94b81c771a32bccbb5e3fb.png)
a végállapotot jelölje 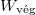 , amikkel:
, amikkel:
![\[ \Delta S \]](/images/math/7/6/0/760ed333dba06ef59d9b2ac749e4bba6.png)
... folyt ...
Ezért az entrópiadefiníciót ki kell egészítenünk a megkülönböztethetetlenséggel, azaz azonos anyagi minőségű részecskék permutációja nem vezet új makroállapothoz:
![\[ S^* = k \ln\frac{W}{N!} \]](/images/math/4/0/8/408a9d7c293cbfb7b9b26c8f550366de.png)
Megjegyzés 2
Találkozhatunk olyan levezetéssel, ami a tartályokat további képzeletbeli egységekre bontja, és a azonos fajtájú gázra számszerűen helyes eredményt ad. Ezt a levezetést alább közöljük, de kevésbé ajánljuk, mert nem tisztázza a megkülönböztethetetlenség kérdését, ugyanakkor a formalizmust feleslegesen bonyolítja.
Legyen azonos fajtájú gáz van mindkét tartályban, a Boltzmann-féle entrópiával számolunk.
Az első tartályt 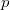 , a másodikat
, a másodikat 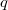 darab cellára osztjuk fel, amelyekben rendre
darab cellára osztjuk fel, amelyekben rendre 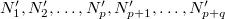 részecske van. Ezt a makroállapotot a fal elvétele előtt
részecske van. Ezt a makroállapotot a fal elvétele előtt 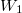 -féle mikroállapot valósíthatja meg. Az
-féle mikroállapot valósíthatja meg. Az 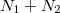 darab részecskét – mivel azok azonos fajtájúak – a két edényben rendelkezésre álló
darab részecskét – mivel azok azonos fajtájúak – a két edényben rendelkezésre álló 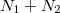 helyükre
helyükre 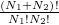 -féleképpen oszthatjuk szét. Majd ezeket az adott edényükben levő cellákban is szét kell osztanunk:
-féleképpen oszthatjuk szét. Majd ezeket az adott edényükben levő cellákban is szét kell osztanunk:
![\[ W_1=\frac{\left( N_1+ N_2\right)!}{N_1! N_2!}\cdot \frac{N_1!}{\prod _{i=1}^pN{\,\mathrm '}_i!}\cdot \frac{N_2!}{\prod _{i=p+1}^{p+q}N{\,\mathrm '}_i!}=\frac{\left( N_1+ N_2\right)!}{\prod _{i=1}^{p+q}N{\,\mathrm '}_i!}.\]](/images/math/1/d/b/1db5d46aec85ca7aa6b9891b1e975b13.png)
A fal felnyitását követően is osszuk fel az egybenyitott edényeket az előbbi makroállapotnak megfelelően (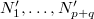 ). Ekkor a
). Ekkor a 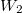 termodinamikai valószínűség:
termodinamikai valószínűség:
![\[ W_2=\frac{\left( N_1+ N_2\right)!}{\prod _{i=1}^{p+q}N{\,\mathrm '}_i!}.\]](/images/math/5/b/d/5bd34c8daacc84163a3b018ef5b05635.png)
Ezekkel a Boltzmann-féle entrópia:
![\[\Delta S=k\ln \frac{W_2}{W_1}=0.\]](/images/math/c/a/e/cae094d47fe009a5422ee28570c4f985.png)
Ha kezdetben a két edényben különböző gázok volnának, akkor 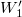 -ben az
-ben az 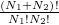 tényező eltűnne, hiszen csak egyféleképpen tudnánk szétosztani a részecskéket a tartályok között. Ekkor:
tényező eltűnne, hiszen csak egyféleképpen tudnánk szétosztani a részecskéket a tartályok között. Ekkor:
![\[\Delta S=k\ln \frac{W_2}{W_1}=k\ln \frac{\left( N_1+ N_2\right)!}{N_1! N_2!}.\]](/images/math/7/8/1/78103971d75dd6a0f3f9546ea451b340.png)
Vegyük észre, hogy a fal felnyitása előtt és után ugyanannyi részecske volt az egyes képzeletbeli cellákban, ez csak egyensúlyban, makroszkopikusan nagy cellákra igaz. Vegyük még észre, hogy élhetünk a 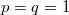 választással, ekkor azonos fajtájú gázra
választással, ekkor azonos fajtájú gázra 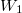 és
és 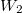 már az egyszerűsítés előtt ugyanazt az alakot ölti, ami a gázrészecskék egymás közötti teljes felcserélhetőségére utal, ami a kezdőállapotban kvantummechanikailag nem is igaz; különböző fajtájú gázokra
már az egyszerűsítés előtt ugyanazt az alakot ölti, ami a gázrészecskék egymás közötti teljes felcserélhetőségére utal, ami a kezdőállapotban kvantummechanikailag nem is igaz; különböző fajtájú gázokra 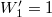 és
és 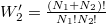 , amit könnyebben magyarázhatunk a megkülönböztethetőséggel.
, amit könnyebben magyarázhatunk a megkülönböztethetőséggel.