„Termodinamika példák - Van der Waals-gáz fajhőkülönbsége” változatai közötti eltérés
A Fizipedia wikiből
(→Megoldás) |
a (Tördelés fejlesztése.) |
||
| (egy szerkesztő 2 közbeeső változata nincs mutatva) | |||
| 9. sor: | 9. sor: | ||
}} | }} | ||
== Feladat == | == Feladat == | ||
| − | </noinclude><wlatex># Fejezzük ki a $C_p-C_V$ különbséget $n$ mol Van der Waals-gáz esetén a hőmérséklet, a térfogat és a $\beta_p$ hőtágulási együttható segítségével!</wlatex><includeonly><wlatex>{{Útmutatás|content=Használjuk fel az általános $$C_p-C_V=\frac{1}{n}\left(p+\left(\frac{\partial U}{\partial V}\right)_T\right)\left(\frac{\partial V}{\partial T}\right)_p$$ egyenletet, a Van der Waals-gáz belső energiájára vonatkozó összefüggést és a hőtágulási együttható definícióját.}}{{Végeredmény|content=$$C_p-C_V=\frac{RT\beta_p}{1-nb/V}.$$}}</wlatex></includeonly><noinclude> | + | </noinclude><wlatex># Fejezzük ki a $C_p-C_V$ különbséget $n$ mol ''Van der Waals''-gáz esetén a hőmérséklet, a térfogat és a $\beta_p$ hőtágulási együttható segítségével!</wlatex><includeonly><wlatex>{{Útmutatás|content=Használjuk fel az általános $$C_p-C_V=\frac{1}{n}\left(p+\left(\frac{\partial U}{\partial V}\right)_T\right)\left(\frac{\partial V}{\partial T}\right)_p$$ egyenletet, a Van der Waals-gáz belső energiájára vonatkozó összefüggést és a hőtágulási együttható definícióját.}}{{Végeredmény|content=$$C_p-C_V=\frac{RT\beta_p}{1-nb/V}.$$}}</wlatex></includeonly><noinclude> |
| + | |||
== Megoldás == | == Megoldás == | ||
| − | <wlatex>A termodinamika első főtételébe ($\delta Q = \mathrm{d}U + p\mathrm{d}V$) behelyettesítve az $U(T,V)$ kétváltozós függvény teljes differenciálját | + | <wlatex>A termodinamika első főtételébe ($\delta Q = \mathrm{d}U + p\,\mathrm{d}V$) behelyettesítve az $U(T,V)$ kétváltozós függvény teljes differenciálját |
| − | $$ \delta Q = \left | + | $$ \delta Q = \left[ p + \left(\frac{\partial U}{\partial V}\right)_T \right] \,\mathrm{d}V + \left(\frac{\partial U}{\partial T}\right)_V \,\mathrm{d}T $$ |
| − | összefüggéshez, és ezt állandó nyomáson | + | összefüggéshez, és ezt állandó nyomáson $\mathrm{d}T$-vel formálisan osztva és a mólhők definícióját alkalmazva |
| − | $$ C_p- C_V=\frac 1 n\left | + | $$ C_p- C_V = \frac{1}{n} \left[ p + \left(\frac{\partial U}{\partial V}\right)_T \right] \left(\frac{\partial V}{\partial T}\right)_p $$ |
általános fajhőösszefüggéshez jutunk. | általános fajhőösszefüggéshez jutunk. | ||
| − | + | A ''Van der Waals''-gáz belső energiáját leíró | |
| − | $$ U=n | + | $$ U = n C_V T - n^2\frac{a}{V} $$ |
| − | + | képletből kiszámíthatjuk | |
| − | $$ | + | $$ \left(\frac{\partial U}{\partial V}\right)_T = \frac{n^2a}{V^2} $$ |
| − | differenciálhányadost | + | differenciálhányadost, és |
$$ \beta_p = \frac{1}{V} \left(\frac{\partial V}{\partial T}\right)_p $$ | $$ \beta_p = \frac{1}{V} \left(\frac{\partial V}{\partial T}\right)_p $$ | ||
definíciót beírhatjuk a fajhőösszefüggésbe: | definíciót beírhatjuk a fajhőösszefüggésbe: | ||
| − | $$ C_p-C_V=\frac{1}{n} \left(p+\frac{n^2a}{V^2}\right) V \beta_p $$ | + | $$ C_p-C_V = \frac{1}{n} \left(p+\frac{n^2a}{V^2}\right) V \beta_p. $$ |
A | A | ||
| − | $$ \left(p+\frac{n^2a}{V^2}\right)\left(V-nb\right)=nRT $$ | + | $$ \left(p+\frac{n^2a}{V^2}\right)\left(V-nb\right) = nRT $$ |
| − | + | Van der Waals-gáz állapotegyenletből az első tényezőt kifejezve egyszerűbb kifejezéshez kapunk: | |
| − | $$ C_p- C_V=\frac{RT | + | $$ C_p-C_V = \frac{RT \beta_p}{\displaystyle 1-\frac{nb}{V}}. $$ |
</wlatex> | </wlatex> | ||
</noinclude> | </noinclude> | ||
A lap jelenlegi, 2013. július 1., 14:54-kori változata
Feladat
- Fejezzük ki a
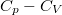 különbséget
különbséget 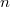 mol Van der Waals-gáz esetén a hőmérséklet, a térfogat és a
mol Van der Waals-gáz esetén a hőmérséklet, a térfogat és a 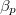 hőtágulási együttható segítségével!
hőtágulási együttható segítségével!
Megoldás
A termodinamika első főtételébe (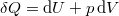 ) behelyettesítve az
) behelyettesítve az 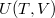 kétváltozós függvény teljes differenciálját
kétváltozós függvény teljes differenciálját
![\[ \delta Q = \left[ p + \left(\frac{\partial U}{\partial V}\right)_T \right] \,\mathrm{d}V + \left(\frac{\partial U}{\partial T}\right)_V \,\mathrm{d}T \]](/images/math/4/7/e/47e28e4d2ecb0595a776271f2fd8433b.png)
összefüggéshez, és ezt állandó nyomáson 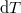 -vel formálisan osztva és a mólhők definícióját alkalmazva
-vel formálisan osztva és a mólhők definícióját alkalmazva
![\[ C_p- C_V = \frac{1}{n} \left[ p + \left(\frac{\partial U}{\partial V}\right)_T \right] \left(\frac{\partial V}{\partial T}\right)_p \]](/images/math/4/9/f/49fc1a0a58730f3ff5d1987ee330e6bf.png)
általános fajhőösszefüggéshez jutunk.
A Van der Waals-gáz belső energiáját leíró
![\[ U = n C_V T - n^2\frac{a}{V} \]](/images/math/5/6/6/56649fa9241afb399b4de7f1a348c9f3.png)
képletből kiszámíthatjuk
![\[ \left(\frac{\partial U}{\partial V}\right)_T = \frac{n^2a}{V^2} \]](/images/math/8/f/3/8f30c8ae997afcfbbc4f1521f522564c.png)
differenciálhányadost, és
![\[ \beta_p = \frac{1}{V} \left(\frac{\partial V}{\partial T}\right)_p \]](/images/math/c/5/b/c5bbb1f2f4680cbba379057eed004602.png)
definíciót beírhatjuk a fajhőösszefüggésbe:
![\[ C_p-C_V = \frac{1}{n} \left(p+\frac{n^2a}{V^2}\right) V \beta_p. \]](/images/math/0/a/3/0a382d8f209fd5bc7d12378a9b2dd02e.png)
A
![\[ \left(p+\frac{n^2a}{V^2}\right)\left(V-nb\right) = nRT \]](/images/math/e/9/d/e9d1173dc59a868ba08a25db27949ea0.png)
Van der Waals-gáz állapotegyenletből az első tényezőt kifejezve egyszerűbb kifejezéshez kapunk:
![\[ C_p-C_V = \frac{RT \beta_p}{\displaystyle 1-\frac{nb}{V}}. \]](/images/math/d/0/0/d000ed3518d8af2ee4ec1b59a3ffd611.png)