Termodinamika példák - Gázcsere tartályok közt
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Termodinamika - Kinetikus gázelmélet, transzportfolyamatok |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Két azonos térfogatú tartály kacsolódik egymáshoz, a szabad úthosszhoz képest kisméretű nyíláson keresztül. Az egyikben
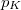 nyomású hidrogéngáz, a másikban kétszer akkora nyomású hidrogéngáz van. A gázok
nyomású hidrogéngáz, a másikban kétszer akkora nyomású hidrogéngáz van. A gázok  hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos
hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos 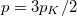 egyensúlyi nyomás alakul ki!
egyensúlyi nyomás alakul ki!
Megoldás
Amikor a gázcsere kis lyukon keresztül valósul meg a tartályok között, feltehetjük, hogy a gáz egy-egy tartályon belül végig egyensúlyi állapotban marad. Ha a lyuk mérete kisebb az átlagos szabad úthossznál, akkor a rajta keresztül időegység alatt távozó molekulák száma pedig megegyezik azzal, az azonos méretű tartályfalának ütközik egységnyi idő alatt. A molekulák száma az egyes tartályokban időben változik, ezt differenciálegyenlet-rendszerrel írhatjuk le:
![\[ \frac{\mathrm{d}N^{(1)}}{\mathrm{d}t} = - \frac14 n_V^{(1)}\langle v \rangle A + \frac14 n_V^{(2)}\langle v \rangle A,\]](/images/math/b/3/4/b347c9f105aeb903ab882413b764b9f2.png)
a molekulák átlagos sebessége 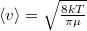 érelmében azonos, hiszen a két tartály hőmérséklete és töltőanyaga is azonos.
érelmében azonos, hiszen a két tartály hőmérséklete és töltőanyaga is azonos.
Az anyagmegmaradás értelmében a második tartályban levő molekulák száma 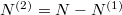 , aminek értelmében
, aminek értelmében 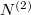 megváltozása is kifejezhető az előző mennyiségekkel:
megváltozása is kifejezhető az előző mennyiségekkel:
![\[ \frac{\mathrm{d}N^{(1)}}{\mathrm{d}t} = -\frac{\mathrm{d}N^{(2)}}{\mathrm{d}t}. \]](/images/math/1/6/c/16c0565dd0bb4bb61f994f9bde059e3a.png)
Felhasználva ezt és, hogy 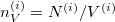 , ismét szétválasztható differenciálegyenletet kapunk:
, ismét szétválasztható differenciálegyenletet kapunk:
![\[ \frac{\mathrm{d}N^{(1)}}{\mathrm{d}t} = - \frac14 \langle v \rangle A \left(\frac1{V^{(1)}}+\frac1{V^{(2)}}\right)N^{(1)} + \frac14 \langle v \rangle A \frac{N}{V^{(2)}}\]](/images/math/c/c/3/cc3d00aae5450695cf80417461abf0c5.png)
Egyensúly esetén 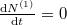 :
:
![\[ \left(\frac1{V^{(1)}}+\frac1{V^{(2)}}\right)N^{(1)} = \frac{N}{V^{(2)}},\]](/images/math/b/0/f/b0f966a77ade8a6c7156ca563e00a791.png)
amiből
![\[ N^{(1)} = \]](/images/math/3/c/9/3c94dd1ab3c2c497790e358b70125cff.png)
Diszkusszió