Termodinamika példák - Átalakulási hő állandó nyomáson
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. május 24., 19:58-kor történt szerkesztése után volt.
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Fázisátalakulások |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Mutassuk meg, hogy mechanikai- és termikus kölcsönhatásban részt vevő rendszerben állandó nyomáson végbemenő fázisátalakulásnál az átalakulási hő (
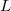 ) az entalpiaváltozással (
) az entalpiaváltozással (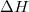 ) egyenlő!
) egyenlő!
Megoldás
Az első főtétel alapján
![\[ \mathrm{d}U=\delta Q-p\,\mathrm{d}V, \]](/images/math/f/e/9/fe9b131e15deeb42877d2d172b821460.png)
amit összehasonlítunk a 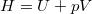 definícióból adódó
definícióból adódó
![\[ \mathrm{d}U = \mathrm{d}H -p\,\mathrm{d}V - V\,\mathrm{d}p\]](/images/math/7/1/d/71d81546fe67b6ce8caae31860e9bbd1.png)
kifejezéssel.
Állandó nyomáson tehát
![\[ \delta Q = \mathrm{d}H, \]](/images/math/7/3/7/73716641e99f86e75d0cf100edd3c2ea.png)
amit a fázisátalakulásra kiintegrálva
![\[ L=\Delta H. \]](/images/math/b/0/2/b0292ab2746abf0d1420ebcb978fa64d.png)