Termodinamika példák - Fázisok egyensúlya szabadenergiával
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. április 21., 17:13-kor történt szerkesztése után volt.
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Fázisátalakulások |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Egy homogén anyag adott hőmérsékleten két fázisban (
 és
és 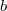 ) létezhet. Az egyes fázisok moláris szabad energiáinak térfogattól való függése (rögzített hőmérsékleten, állandó anyagmennyiség esetén) az ábrán látható.
) létezhet. Az egyes fázisok moláris szabad energiáinak térfogattól való függése (rögzített hőmérsékleten, állandó anyagmennyiség esetén) az ábrán látható.
Mutassuk ki, hogy egyensúlyi állapotban a fázisok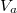 és
és 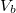 térfogatai a két görbéhez húzott közös érintő érintési pontjainak abszcisszái, a közös nyomás pedig az érintő negatív iránytangense!
térfogatai a két görbéhez húzott közös érintő érintési pontjainak abszcisszái, a közös nyomás pedig az érintő negatív iránytangense!
Megoldás
Egyensúlyban 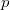 ,
,  ,
, 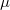 azonos a két fázisban. A szabadenergiára alkalmazható differenciális összefüggés:
azonos a két fázisban. A szabadenergiára alkalmazható differenciális összefüggés:
![\[ \left(\frac{\partial F}{\partial V}\right)_T = \left(\frac{\partial F_M}{\partial V_M}\right)_T = -p \]](/images/math/a/a/0/aa0c8c23937d7cc2dba2d2a86320ba66.png)
Mivel mindkét fázisban azonos a nyomás:
![\[ \left(\frac{\partial F_{Ma}}{\partial V_{M}}\right)_T = \left(\frac{\partial F_{Mb}}{\partial V_{M}}\right)_T = -p, \]](/images/math/8/b/4/8b49a47816bc9253795dde71ac955640.png)
azaz  és
és 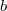 fázis görbééin az egyensúly által kiválasztott egy-egy pont érintőinek a meredeksége azonos, a pontbeli érintők párhuzamosak.
fázis görbééin az egyensúly által kiválasztott egy-egy pont érintőinek a meredeksége azonos, a pontbeli érintők párhuzamosak.
Fejezzük ki a kémiai potenciált a megadott mennyiségekkel:
![\[ G=\mu n=F+pV, \qquad \mu = F_M+p V_M. \]](/images/math/5/f/e/5febb2b4e04b174c48515e7a01156f22.png)
Mivel mindkét fázisban azonos a kémiai potenciál és a nyomás:
![\[ -p = \frac{F_{Mb}- F_{Ma}}{V_{Mb}- V_{Ma}}, \]](/images/math/1/c/1/1c12a5029c560b385508da3697eb8873.png)
azaz  és
és 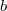 fázis görbéin az egyensúly által kiválasztott egy-egy pontot összekötő egyenes meredeksége is azonos kell legyen az előzőleg vizsgált két érintő egyenessel. Ezen három egyenes pedig csak a feladatban leírt esetben párhuzamosak.
fázis görbéin az egyensúly által kiválasztott egy-egy pontot összekötő egyenes meredeksége is azonos kell legyen az előzőleg vizsgált két érintő egyenessel. Ezen három egyenes pedig csak a feladatban leírt esetben párhuzamosak.
Megjegyzés
Egy kiválasztott 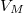 móltérfogat kijelöli az egyensúlyban a fázisok arányát:
móltérfogat kijelöli az egyensúlyban a fázisok arányát:
- ha
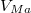 alatt van, csak az
alatt van, csak az  fázis lesz jelen
fázis lesz jelen
- ha
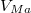 felett és
felett és 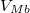 alatt van, mindkét fázis jelen lesz, az
alatt van, mindkét fázis jelen lesz, az  fázis
fázis 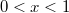 , a
, a 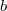 fázis
fázis 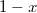 részben alkotja a rendszert, hogy
részben alkotja a rendszert, hogy 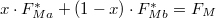 és
és 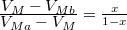
- ha
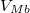 felett van, csak a
felett van, csak a 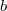 fázis lesz jelen
fázis lesz jelen