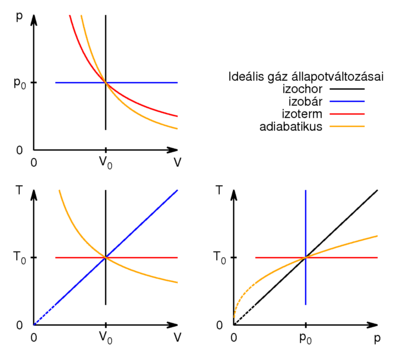Termodinamika példák - Állapotváltozások diagramjai
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. április 6., 16:57-kor történt szerkesztése után volt.
Feladat
- Készítsen vázlatos ábrát ideális gáz
- a) izochor,
- b) izobár,
- c) izoterm és
- d) adiabatikus
- állapotváltozásáról
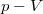 ,
, 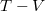 és
és 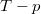 koordináta-rendszerekben úgy, hogy a kiindulási állapot minden esetben ugyanaz legyen!
koordináta-rendszerekben úgy, hogy a kiindulási állapot minden esetben ugyanaz legyen!
Megoldás
- A görbék megszerkesztéséhez
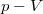 diagramban
diagramban 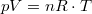 állapotegyenletből, és a
állapotegyenletből, és a 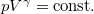 adiabatita egyenletéből indulunk ki,
adiabatita egyenletéből indulunk ki, 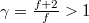 .
.
-
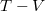 diagramban az adiabata egyenletét
diagramban az adiabata egyenletét 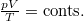 egyenletel osztva
egyenletel osztva 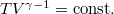 görbét ábrázoljuk.
görbét ábrázoljuk.
-
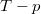 diagramban az előző egyenletet
diagramban az előző egyenletet 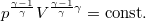 egyenlettel osztva
egyenlettel osztva 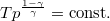 ábrázolandó összefüggést nyerjük.
ábrázolandó összefüggést nyerjük.
Fontos megfigyelni, melyik görbe milyen meredekséggel érkezik (elméletben) az origóba.