Termodinamika példák - Argon olvadási görbéje
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. április 21., 16:10-kor történt szerkesztése után volt.
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Fázisátalakulások |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- A szilárd argon
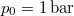 nyomáson
nyomáson 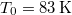 hőmérsékleten olvad meg. Olvadáshője ekkor
hőmérsékleten olvad meg. Olvadáshője ekkor 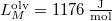 , móltérfogatának változása
, móltérfogatának változása 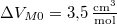 . A nyomás növekedésekor az olvadáshő nem változik, a
. A nyomás növekedésekor az olvadáshő nem változik, a 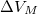 móltérfogatváltozás viszont az abszolút hőmérséklet
móltérfogatváltozás viszont az abszolút hőmérséklet 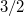 -ik hatványával arányos.
-ik hatványával arányos.
Mekkora nyomást kell alkalmaznunk ahhoz, hogy az olvadási hőmérséklet megkétszereződjék?
Megoldás
A móltérfogat
![\[ \Delta V_M = \Delta V_{M0} \left(\frac{T}{T_0}\right)^{\frac32} \]](/images/math/2/d/8/2d8f277b29dac51bd5fa5f945d1383df.png)
hőmérsékletfüggését behelyettesítjük a Clapeyron-egyenletbe
![\[ \frac{\mathrm{d}p}{\mathrm{d}T} = \frac{L_M^\text{olv} T_0^{\frac32}}{T^{\frac52} \Delta V_{M0}^\text{olv}}, \]](/images/math/0/5/6/05660b427253335102bdbcdfbdb8a6cf.png)
majd változószétválasztás után integrálva 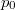 és
és 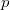 illetve
illetve 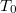 és
és 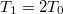 között:
között:
![\[ p = p_0+\frac{L_M^\text{olv} T_0^{\frac32}}{\Delta V_{M0}} \left[-\frac23 T^{-\frac32}\right]_{T_0}^{2 T_0} = p_0+\frac23\frac{L_M^\text{olv}}{\Delta V_{M0}}\left(1-\left(\frac12\right)^{\frac32}\right) \approx 1449{,}04\,\mathrm{bar}. \]](/images/math/5/8/0/5800e3d57365b7ec70e4340f7d0937c7.png)