„Termodinamika példák - Belső energia az állapotváltozások során” változatai közötti eltérés
A Fizipedia wikiből
| 19. sor: | 19. sor: | ||
<wlatex>A belső energia felírásához az $U=\frac{f}{2}NkT$ ekvipartíció tételét, a $pV=NkT$ állapotegyenletet és az adiabata egyenletét használjuk. | <wlatex>A belső energia felírásához az $U=\frac{f}{2}NkT$ ekvipartíció tételét, a $pV=NkT$ állapotegyenletet és az adiabata egyenletét használjuk. | ||
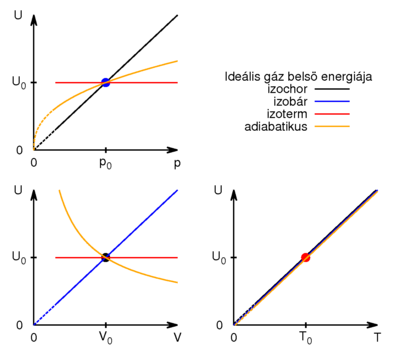
* $U-T$ diagramon a belső energia csak a hőmérséklet függvénye, minden görbe egybeesik, az izoterm állapotváltozáshoz rögzített részecskeszám esetén egyetlen pont tartozik. | * $U-T$ diagramon a belső energia csak a hőmérséklet függvénye, minden görbe egybeesik, az izoterm állapotváltozáshoz rögzített részecskeszám esetén egyetlen pont tartozik. | ||
| − | * $U-V$ diagramon az adiabata $pV^\gamma=\mathrm{const.}$ egyenletéből $pV=\mathrm{const.}\cdot V^{1-\gamma}$ és $U=\mathrm{const.}\cdot V^{1-\gamma}$ egyenletet vezethetjük le, $\gamma=frac{f+2}{f}>1$. | + | * $U-V$ diagramon az adiabata $pV^\gamma=\mathrm{const.}$ egyenletéből $pV=\mathrm{const.}\cdot V^{1-\gamma}$ és $U=\mathrm{const.}\cdot V^{1-\gamma}$ egyenletet vezethetjük le, $\gamma=\frac{f+2}{f}>1$. |
* $U-p$ diagramon az adiabata $p^{1-\gamma}{\gamma}T=\mathrm{const.}$ egyenletéből $U=\mathit{all}\cdot p^{1-\frac{1}{\gamma}}$ összefüggést kapjuk. | * $U-p$ diagramon az adiabata $p^{1-\gamma}{\gamma}T=\mathrm{const.}$ egyenletéből $U=\mathit{all}\cdot p^{1-\frac{1}{\gamma}}$ összefüggést kapjuk. | ||
Fontos megfigyelni, melyik görbe milyen meredekséggel érkezik (elméletben) az origóba. | Fontos megfigyelni, melyik görbe milyen meredekséggel érkezik (elméletben) az origóba. | ||
| − | [[Fájl:Belső energia állapotváltozások során.png]] | + | [[Fájl:Belső energia állapotváltozások során.png|400px]] |
</wlatex> | </wlatex> | ||
</noinclude> | </noinclude> | ||
A lap 2013. április 6., 17:50-kori változata
| Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Állapotváltozás, I. főtétel |
Feladatok listája:
|
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Ábrázolja vázlatosan ideális gáz
- a) izochor,
- b) izobár,
- c) izoterm és
- d) adiabatikus
- állapotváltozásánál a belső energiának a hőmérséklettől-, térfogattól- és a nyomástól való függését! Legyen a belső energia az ordináta, és minden folyamatnál legyen ugyanaz a kiindulási állapot!
Megoldás
A belső energia felírásához az 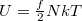 ekvipartíció tételét, a
ekvipartíció tételét, a 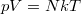 állapotegyenletet és az adiabata egyenletét használjuk.
állapotegyenletet és az adiabata egyenletét használjuk.
-
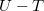 diagramon a belső energia csak a hőmérséklet függvénye, minden görbe egybeesik, az izoterm állapotváltozáshoz rögzített részecskeszám esetén egyetlen pont tartozik.
diagramon a belső energia csak a hőmérséklet függvénye, minden görbe egybeesik, az izoterm állapotváltozáshoz rögzített részecskeszám esetén egyetlen pont tartozik.
-
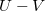 diagramon az adiabata
diagramon az adiabata 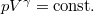 egyenletéből
egyenletéből 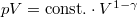 és
és 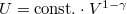 egyenletet vezethetjük le,
egyenletet vezethetjük le, 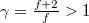 .
.
-
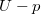 diagramon az adiabata
diagramon az adiabata 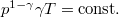 egyenletéből
egyenletéből 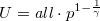 összefüggést kapjuk.
összefüggést kapjuk.
Fontos megfigyelni, melyik görbe milyen meredekséggel érkezik (elméletben) az origóba.