„Kvantummechanikai bevezető példák - Schrödinger-egyenlet megoldása hidrogénatomban” változatai közötti eltérés
a |
a (Tördelés fejlesztése.) |
||
| (egy szerkesztő 4 közbeeső változata nincs mutatva) | |||
| 9. sor: | 9. sor: | ||
}} | }} | ||
== Feladat == | == Feladat == | ||
| − | </noinclude><wlatex># Határozza meg a ''Schrödinger''-féle hidrogénatomban az elektron alapállapoti hullámfüggvényét! Számítsa ki, hogy protontól milyen távolságban található meg az elektron a legnagyobb valószínűséggel!</wlatex><includeonly><wlatex>{{Útmutatás|content=$$ | + | </noinclude><wlatex># Határozza meg a ''Schrödinger''-féle hidrogénatomban az elektron alapállapoti hullámfüggvényét! Számítsa ki, hogy protontól milyen távolságban található meg az elektron a legnagyobb valószínűséggel!</wlatex><includeonly><wlatex>{{Útmutatás|content=Az elektron sugárirányú megtalálási valószínűségének eloszlás $$ R(r) = A_n \left(\frac{r}{a_0}\right)^{n-1} e^{\textstyle -\frac{r}{n a_0}}.$$}}{{Végeredmény|content=$$r_\text{lv.}=n^2 a_0$$}}</wlatex></includeonly><noinclude> |
== Megoldás == | == Megoldás == | ||
| − | <wlatex>A Schrödinger- | + | <wlatex>A hidrogénatom ''Schrödinger''-egyenlete |
$$ -\frac{\hbar^2}{2m}\triangle\Psi + V(r)\Psi = E\Psi, $$ | $$ -\frac{\hbar^2}{2m}\triangle\Psi + V(r)\Psi = E\Psi, $$ | ||
aminek megoldását $\Psi(r,\vartheta,\varphi)=R(r)\Theta(\vartheta)\Phi(\varphi)$ alakban érdemes keresni. A megoldás abszolútértéknégyzete ($|\Psi|^2$) az elektron megtalálási valószínűsége egy adott térfogatelemben. A ''Schrödinger''-egyenlet megoldása a szögfüggő tényezők levezetésével megtalálható a [http://goliat.eik.bme.hu/~tothaf/Tananyagok/Letoltesek/atfiz_bev.pdf kibővített óravázlat] 34-38. oldalán. | aminek megoldását $\Psi(r,\vartheta,\varphi)=R(r)\Theta(\vartheta)\Phi(\varphi)$ alakban érdemes keresni. A megoldás abszolútértéknégyzete ($|\Psi|^2$) az elektron megtalálási valószínűsége egy adott térfogatelemben. A ''Schrödinger''-egyenlet megoldása a szögfüggő tényezők levezetésével megtalálható a [http://goliat.eik.bme.hu/~tothaf/Tananyagok/Letoltesek/atfiz_bev.pdf kibővített óravázlat] 34-38. oldalán. | ||
| 22. sor: | 22. sor: | ||
Az elektron megtalálási valószínűsége $[r,r+\mathrm{d}r]$ intervallumban tehát | Az elektron megtalálási valószínűsége $[r,r+\mathrm{d}r]$ intervallumban tehát | ||
| − | $$ \int_0^{2\pi} \int_0^\pi |\Psi(r,\vartheta,\varphi)|^2 r^2 sin \vartheta \,\mathrm{d}r \,\mathrm{d}\vartheta \,\mathrm{d}\varphi | + | $$ \int_0^{2\pi} \int_0^\pi |\Psi(r,\vartheta,\varphi)|^2 r^2 \sin \vartheta \,\mathrm{d}r \,\mathrm{d}\vartheta \,\mathrm{d}\varphi |
| − | \sim r\cdot R(r)\,\mathrm{d}r $$ | + | \sim \left[r\cdot R(r)\right]^2 \,\mathrm{d}r $$ |
A legvalószínűbb sugarat $r\cdot R(r)$ szélsőértékhelye adja: | A legvalószínűbb sugarat $r\cdot R(r)$ szélsőértékhelye adja: | ||
| − | $$ 0 = \left. \frac{\mathrm{d}}{\mathrm{d}r} \ | + | $$ 0 = \left. \frac{\mathrm{d}}{\mathrm{d}r} \Big(r\cdot R(r)\Big) \right|_{r_\text{lv.}} |
| − | = | + | = A_n \left[ n\left(\frac{r_\text{lv.}}{a_0}\right)^{n-1} - \frac{1}{n}\left(\frac{r_\text{lv.}}{a_0}\right)^n \right] e^{\textstyle -\frac{r_\text{lv.}}{n a_0}}, $$ |
| − | ami alapján $r_\text{ | + | ami alapján $r_\text{lv.}=n^2 a_0$. Az alapállapotú hidrogénatomban a legvalószínűbb sugár éppen a ''Bohr''-sugár. |
</wlatex> | </wlatex> | ||
</noinclude> | </noinclude> | ||
A lap jelenlegi, 2013. június 17., 00:29-kori változata
| Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Kvantummechanikai bevezető |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Határozza meg a Schrödinger-féle hidrogénatomban az elektron alapállapoti hullámfüggvényét! Számítsa ki, hogy protontól milyen távolságban található meg az elektron a legnagyobb valószínűséggel!
Megoldás
A hidrogénatom Schrödinger-egyenlete
![\[ -\frac{\hbar^2}{2m}\triangle\Psi + V(r)\Psi = E\Psi, \]](/images/math/5/6/3/5631fd2ca402df7aca11a96626165bbe.png)
aminek megoldását 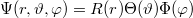 alakban érdemes keresni. A megoldás abszolútértéknégyzete (
alakban érdemes keresni. A megoldás abszolútértéknégyzete (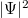 ) az elektron megtalálási valószínűsége egy adott térfogatelemben. A Schrödinger-egyenlet megoldása a szögfüggő tényezők levezetésével megtalálható a kibővített óravázlat 34-38. oldalán.
) az elektron megtalálási valószínűsége egy adott térfogatelemben. A Schrödinger-egyenlet megoldása a szögfüggő tényezők levezetésével megtalálható a kibővített óravázlat 34-38. oldalán.
A sugárirányú differenciálegyenletet 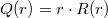 helyettesítéssel megoldva a sugárirányú eloszlás
helyettesítéssel megoldva a sugárirányú eloszlás
![\[ R(r) = A_n \left(\frac{r}{a_0}\right)^{n-1} e^{\textstyle -\frac{r}{n a_0}}, \]](/images/math/9/f/d/9fd3c90ed55f2d0d8ff424777b53c98c.png)
ahol 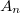 egy, a pályára jellemző normáló tényező, hogy a megtalálási valószínűség teljes térre vett integrálja
egy, a pályára jellemző normáló tényező, hogy a megtalálási valószínűség teljes térre vett integrálja 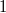 legyen.
A másik két eloszlás értéke a feladat megoldásában nem játszik szerepet, mert a szögek szerint kiintegrálva ugyanazt a sugártól független állandót adják.
legyen.
A másik két eloszlás értéke a feladat megoldásában nem játszik szerepet, mert a szögek szerint kiintegrálva ugyanazt a sugártól független állandót adják.
Az elektron megtalálási valószínűsége ![\setbox0\hbox{$[r,r+\mathrm{d}r]$}% \message{//depth:\the\dp0//}% \box0%](/images/math/b/c/c/bcc8b3a1eda12dfc7239df89d3dee2f8.png) intervallumban tehát
intervallumban tehát
![\[ \int_0^{2\pi} \int_0^\pi |\Psi(r,\vartheta,\varphi)|^2 r^2 \sin \vartheta \,\mathrm{d}r \,\mathrm{d}\vartheta \,\mathrm{d}\varphi \sim \left[r\cdot R(r)\right]^2 \,\mathrm{d}r \]](/images/math/f/6/1/f61673d3b697a2fc76681bbd25e81fee.png)
A legvalószínűbb sugarat 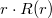 szélsőértékhelye adja:
szélsőértékhelye adja:
![\[ 0 = \left. \frac{\mathrm{d}}{\mathrm{d}r} \Big(r\cdot R(r)\Big) \right|_{r_\text{lv.}} = A_n \left[ n\left(\frac{r_\text{lv.}}{a_0}\right)^{n-1} - \frac{1}{n}\left(\frac{r_\text{lv.}}{a_0}\right)^n \right] e^{\textstyle -\frac{r_\text{lv.}}{n a_0}}, \]](/images/math/0/5/3/053824569620cab57d128596b2a222d0.png)
ami alapján 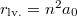 . Az alapállapotú hidrogénatomban a legvalószínűbb sugár éppen a Bohr-sugár.
. Az alapállapotú hidrogénatomban a legvalószínűbb sugár éppen a Bohr-sugár.