Kvantummechanikai bevezető példák - Schrödinger-egyenlet megoldása hidrogénatomban
A Fizipedia wikiből
A lap korábbi változatát látod, amilyen Stippinger (vitalap | szerkesztései) 2013. május 29., 20:13-kor történt szerkesztése után volt.
| [rejt] Navigáció Pt·1·2·3 |
|---|
| Kísérleti fizika 3. gyakorlat |
| Gyakorlatok listája: |
| Kvantummechanikai bevezető |
| Feladatok listája: |
| © 2012-2013 BME-TTK, TÁMOP4.1.2.A/1-11/0064 |
Feladat
- Határozza meg a Schrödinger-féle hidrogénatomban az elektron alapállapoti hullámfüggvényét! Számítsa ki, hogy protontól milyen távolságban található meg az elektron a legnagyobb valószínűséggel!
Megoldás
A Schrödinger-egyenlet megoldása megtalálható a kibővített óravázlat 34-38. oldalán.
A Schrödinger-egyenlet
![\[ -\frac{\hbar^2}{2m}\triangle\Psi + V(r)\Psi = E\Psi, \]](/images/math/5/6/3/5631fd2ca402df7aca11a96626165bbe.png)
aminek megoldását 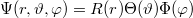 alakban érdemes keresni. A megoldás abszolútértéknégyzete (
alakban érdemes keresni. A megoldás abszolútértéknégyzete (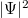 ) az elektron megtalálási valószínűsége. A differenciálegyenletet megoldva a sugárirányú eloszlás
) az elektron megtalálási valószínűsége. A differenciálegyenletet megoldva a sugárirányú eloszlás
![\[ R(r) = A_n \left(\frac{r}{a_0}\right)^{n-1} e^{-\frac{r}{n a_0}}, \]](/images/math/d/8/2/d8263890ac3209cccc87a3fdd921e0d9.png)
ahol 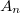 egy, a pályára jellemző normáló tényező, hogy a megtalálási valószínűség teljes térre vett integrálja
egy, a pályára jellemző normáló tényező, hogy a megtalálási valószínűség teljes térre vett integrálja 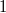 legyen.
A másik két eloszlás értéke a feladat megoldásában nem játszik szerepet, mert a szögek szerint kiintegrálva ugyanazt a sugártól független állandót adják.
legyen.
A másik két eloszlás értéke a feladat megoldásában nem játszik szerepet, mert a szögek szerint kiintegrálva ugyanazt a sugártól független állandót adják.
A legvalószínűbb sugarat 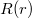 szélsőértékhelye adja:
szélsőértékhelye adja: