Kísérleti fizika 3. gyakorlat: Teljes példasor
A Fizipedia wikiből
Az egyes feladatsorok a legfontosabb képletekkel kiegészítve egyenként is elérhetőek a címekre klikkelve.
Tartalomjegyzék |
Kinetikus gázelmélet, transzportfolyamatok
- Fejezze ki az egyatomos ideális gáz nyomását a gáz
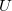 belső energiájával és
belső energiájával és 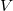 térfogatával!Végeredmény
térfogatával!Végeredmény![\[p=\frac{2U}{3V}\]](/images/math/7/9/a/79a5ef5aee3e9a6d7f09326b91f3a4b4.png)
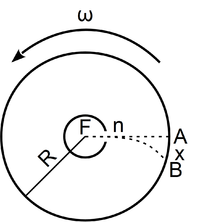
- Stern híres kísérletében, amellyel a Maxwell-eloszlás kísérleti igazolását adta,
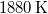 -es ezüstszálról távozó atomok sebességeloszlását mérte meg, az ábrán vázolt elrendezéssel. Az
-es ezüstszálról távozó atomok sebességeloszlását mérte meg, az ábrán vázolt elrendezéssel. Az 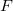 pontbeli tengelyen elhelyezkedő szálról távozó ezüstatomok az
pontbeli tengelyen elhelyezkedő szálról távozó ezüstatomok az 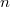 nyíláson át jutottak az
nyíláson át jutottak az 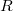 sugarú hengerfelületre. A berendezés
sugarú hengerfelületre. A berendezés  szögsebességgel forgott, aminek következtében a
szögsebességgel forgott, aminek következtében a  sebességű atom az
sebességű atom az 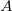 pont helyett
pont helyett 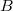 -ben csapódott le.
-ben csapódott le.
- a) Állapítsuk meg az
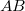 ív
ív  hosszát
hosszát 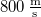 sebességű atomok esetén, ha a fordulatszám
sebességű atomok esetén, ha a fordulatszám 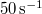 és
és 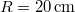 !Végeredmény
!Végeredmény![\[x=\frac{\omega R^2}{v}\]](/images/math/0/b/6/0b64d775cd07f10acdc2f74976361052.png)
- b) Milyen sebességnél adják a legnagyobb rétegvastagságot a külső hengerfelületen lecsapódó ezüstatomok?ÚtmutatásAz időegység alatt lecsapódó részecskék számát határozzuk meg a Maxwell-eloszlás alapján, és használjuk ki az
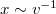 összefüggést. Végeredményahol
összefüggést. Végeredményahol![\[v_m=\sqrt{\frac52}\,v_0,\]](/images/math/b/b/e/bbec4f31fa99ad4b348e8f27cca0b017.png)
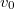 a legvalószínűbb sebesség.
a legvalószínűbb sebesség.
- a) Állapítsuk meg az
- Az
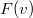 sebességeloszlási függvényből a
sebességeloszlási függvényből a 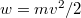 összefüggés felhasználásával vezessük le az
összefüggés felhasználásával vezessük le az 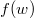 energia-eloszlási függvényt, ahol
energia-eloszlási függvényt, ahol 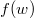 azt mutatja meg, hogy az összes molekula hányadrésze rendelkezik
azt mutatja meg, hogy az összes molekula hányadrésze rendelkezik 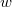 és
és 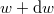 közötti mozgási energiával! Mekkora a legvalószínűbb
közötti mozgási energiával! Mekkora a legvalószínűbb 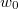 energia és mennyi az átlagos kinetikus energia?Végeredmény
energia és mennyi az átlagos kinetikus energia?Végeredmény![\[f(w)=\frac{4}{v_0\sqrt{\pi}}\frac{1}{w_v\sqrt{2\mu}}\sqrt{w} \exp\left\{ -\frac{w}{w_v} \right\}, \text{ ahol } w_v=\frac12 \mu v_0^2=kT\]](/images/math/4/6/e/46ed18cb6e204a14b7d02f1f6f168d50.png)
![\[w_0=\frac12kT,\qquad \langle w\rangle=\frac32kT\]](/images/math/3/a/7/3a7857f15c6a811008e25cebad3e2a36.png)
- Legfeljebb mekkora lehet az
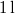 térfogatú, gömb alakú edényben lévő
térfogatú, gömb alakú edényben lévő 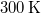 -es hidrogéngáz nyomása, hogy az átlagos szabad úthossz nagyobb legyen az edény átmérőjénél? A hidrogénmolekula átmérője
-es hidrogéngáz nyomása, hogy az átlagos szabad úthossz nagyobb legyen az edény átmérőjénél? A hidrogénmolekula átmérője 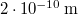 .Végeredményahol
.Végeredményahol![\[p<\frac{kT}{2\sqrt{2}\, R \, d^2\pi}=0{,}188\,\mathrm{Pa},\]](/images/math/f/1/3/f13f6dbd41c6c990671c0eb82ccfe194.png)
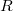 az
az 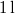 -es tartály sugara.
-es tartály sugara.
- Hogyan változik az ideális gáz
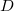 diffúziós állandója és
diffúziós állandója és 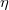 belső súrlódási együtthatója, ha a gáz térfogata
belső súrlódási együtthatója, ha a gáz térfogata 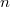 -szersére nő
-szersére nő
- a) állandó hőmérsékleten,Végeredmény
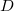
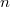 -szeres,
-szeres, 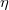 változatlan.
változatlan. - b) állandó nyomáson?Végeredmény
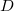
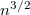 -szeres,
-szeres, 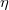
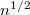 -szeres.
-szeres.
- a) állandó hőmérsékleten,
-
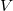 térfogatú, vékonyfalú tartályban ideális gáz van, az edényt légüres tér veszi körül. Feltesszük, hogy a gáz kiáramlása lassú, így a gáz egyensúlyi állapotát a folyamat nem zavarja, továbbá a lyuk mérete sokkal kisebb, mint a szabad úthossz, tehát a lyuk területére is érvényes az az összefüggés, hogy az edény falának időegység alatt nekiütköző molekulák száma
térfogatú, vékonyfalú tartályban ideális gáz van, az edényt légüres tér veszi körül. Feltesszük, hogy a gáz kiáramlása lassú, így a gáz egyensúlyi állapotát a folyamat nem zavarja, továbbá a lyuk mérete sokkal kisebb, mint a szabad úthossz, tehát a lyuk területére is érvényes az az összefüggés, hogy az edény falának időegység alatt nekiütköző molekulák száma 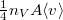 , ahol
, ahol 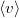 a molekulák átlagsebessége. A hőmérséklet mindvégig
a molekulák átlagsebessége. A hőmérséklet mindvégig  .
.
- a) Hogyan változik az idő függvényében az edényben lévő gáz
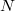 részecskeszáma, ha a tartály falán igen kicsi,
részecskeszáma, ha a tartály falán igen kicsi, 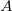 területű lyuk van?Végeredményahol
területű lyuk van?Végeredményahol![\[N(t)=n_0\exp\{-t/\tau\},\]](/images/math/0/f/6/0f66732b3648dd5d9e4a439bd08de0d9.png)
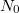 a kezdeti részecskeszám-sűrűség,
a kezdeti részecskeszám-sűrűség, 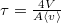 .
. - b) Határozzuk meg azt az időtartamot, amely alatt a gáz nyomása felére csökken!Végeredmény
![\[\tau_{1/2}=\tau \ln 2\]](/images/math/8/9/8/8988e91daa948b7308b8d2c1d7b6f229.png)
- a) Hogyan változik az idő függvényében az edényben lévő gáz
- Két azonos térfogatú tartály kacsolódik egymáshoz, a szabad úthosszhoz képest kisméretű nyíláson keresztül. Az egyikben
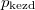 nyomású, a másikban kétszer akkora nyomású hidrogéngáz van. A gázok
nyomású, a másikban kétszer akkora nyomású hidrogéngáz van. A gázok  hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos
hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos 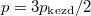 egyensúlyi nyomás alakul ki!ÚtmutatásHasználjuk ki, hogy egyensúlyban az egyes edényekben a molekulák térfogati sűrűsége állandó, és az összes molekulák száma a folyamatban nem változik.
egyensúlyi nyomás alakul ki!ÚtmutatásHasználjuk ki, hogy egyensúlyban az egyes edényekben a molekulák térfogati sűrűsége állandó, és az összes molekulák száma a folyamatban nem változik.
- Két azonos térfogatú tartály kacsolódik egymáshoz, a szabad úthosszhoz képest kisméretű nyíláson keresztül. Az egyikben
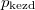 nyomású hidrogéngáz, a másikban kétszer akkora nyomású oxigéngáz van. A gázok
nyomású hidrogéngáz, a másikban kétszer akkora nyomású oxigéngáz van. A gázok  hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos
hőmérséklete azonos és időben állandó. A kinetikus gázelmélet segítségével mutassuk ki, hogy a két tartályban azonos 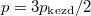 egyensúlyi nyomás alakul ki!ÚtmutatásHasználjuk ki, hogy a két gáz nem hat kölcsön, alkalmazzuk a parciális nyomások tételét.
egyensúlyi nyomás alakul ki!ÚtmutatásHasználjuk ki, hogy a két gáz nem hat kölcsön, alkalmazzuk a parciális nyomások tételét.
- Egy
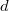 vastagságú, nagy felületű, homogén anyagréteg két ellentétes felületén a hőmérséklet állandó
vastagságú, nagy felületű, homogén anyagréteg két ellentétes felületén a hőmérséklet állandó  és
és 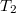 , az anyag hővezetési tényezője hőmérséklet- és helyfüggetlen. A hővezetés alapegyenlete segítségével mutassuk ki, hogy a rétegben a hőmérséklet lineárisan változik az egyik felülettől mért
, az anyag hővezetési tényezője hőmérséklet- és helyfüggetlen. A hővezetés alapegyenlete segítségével mutassuk ki, hogy a rétegben a hőmérséklet lineárisan változik az egyik felülettől mért  távolsággal, és írjuk fel a
távolsággal, és írjuk fel a 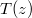 függvényt a megadott mennyiségekkel!Végeredmény
függvényt a megadott mennyiségekkel!Végeredmény![\[T(z)=T_1+\frac{T_2-T_1}{d}z\]](/images/math/b/6/5/b6576fbfcb4cdb76f8702fbc59f78dae.png)
- Mennyi idő alatt képződik
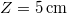 vastag jégréteg egy tó felszínén, ha a léghőmérséklet
vastag jégréteg egy tó felszínén, ha a léghőmérséklet 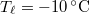 , a víz hőmérséklete a jégréteg alatt
, a víz hőmérséklete a jégréteg alatt 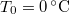 ? Tegyük fel, hogy a jégréteg felső felülete mindig azonos hőmérsékletű a levegővel, alső felülete pedig mindig
? Tegyük fel, hogy a jégréteg felső felülete mindig azonos hőmérsékletű a levegővel, alső felülete pedig mindig 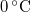 -os. A jég olvadáshője
-os. A jég olvadáshője 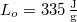 , hővezetési tényezője
, hővezetési tényezője 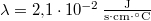 , sűrűsége pedig
, sűrűsége pedig 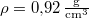 .ÚtmutatásÍrjuk fel egy elemi időtartam alatt keletkező elemi vastagságú jégréteg felszabadulásakor keletkező hőt, és tegyük fel, hogy ez a jégrétegen keresztül hővezetéssel távozik, majd integráljuk a kapott egyenletet. Az analitikus megoldás érdekében hanyagoljuk el a jég fajhőjét.Végeredmény5 óra alatt képződik
.ÚtmutatásÍrjuk fel egy elemi időtartam alatt keletkező elemi vastagságú jégréteg felszabadulásakor keletkező hőt, és tegyük fel, hogy ez a jégrétegen keresztül hővezetéssel távozik, majd integráljuk a kapott egyenletet. Az analitikus megoldás érdekében hanyagoljuk el a jég fajhőjét.Végeredmény5 óra alatt képződik![\[t(Z) = \left(\frac{\rho L_o}{2\lambda(T_0-T_\ell)}\right)\,Z^2, \]](/images/math/d/8/7/d876a0a553d038419a342caf35cbffed.png)
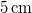 vastag jégréteg.
vastag jégréteg.
-
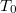 hőmérsékletű, igen nagy hőkapacitású folyadékba
hőmérsékletű, igen nagy hőkapacitású folyadékba 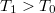 hőmérsékletű,
hőmérsékletű, 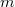 tömegű és
tömegű és  fajhőjű, abszolút jó hővezető testet helyezünk a
fajhőjű, abszolút jó hővezető testet helyezünk a 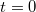 pillanatban. A test lehűlése a Newton-féle lehűlési törvény szerint zajlik (
pillanatban. A test lehűlése a Newton-féle lehűlési törvény szerint zajlik (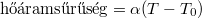 ), az
), az 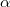 hőátadási tényező ismert, a test felületének nagysága
hőátadási tényező ismert, a test felületének nagysága 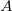 . Határozzuk meg a test hőmérsékletét
. Határozzuk meg a test hőmérsékletét 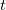 idő eltelte után!ÚtmutatásA leadott hőt fejezzük ki egyrészt a hőkapacitással, és a hőmérsékletváltozással, másrészt a folyadékba történő hőátadással, és integráljuk a kapott egyenletet.Végeredmény
idő eltelte után!ÚtmutatásA leadott hőt fejezzük ki egyrészt a hőkapacitással, és a hőmérsékletváltozással, másrészt a folyadékba történő hőátadással, és integráljuk a kapott egyenletet.Végeredmény![\[T = T_0+\left(T_1-T_0\right)e^{\textstyle -\frac{A\alpha}{cm}t}\]](/images/math/1/3/f/13f20fc241d9d56f3b09002a2987438f.png)
Állapotváltozás, I. főtétel
- Készítsen vázlatos ábrát ideális gáz
- a) izochor,
- b) izobár,
- c) izoterm és
- d) adiabatikus
- állapotváltozásáról
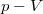 ,
, 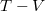 és
és 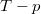 koordináta-rendszerekben úgy, hogy a kiindulási állapot minden esetben ugyanaz legyen!
koordináta-rendszerekben úgy, hogy a kiindulási állapot minden esetben ugyanaz legyen!
- Ábrázolja vázlatosan ideális gáz
- a) izochor,
- b) izobár,
- c) izoterm és
- d) adiabatikus
- állapotváltozásánál a belső energiának a hőmérséklettől-, térfogattól- és a nyomástól való függését! Legyen a belső energia az ordináta, és minden folyamatnál legyen ugyanaz a kiindulási állapot!
- Állapítsuk meg, milyen összefüggés van egy ideális gáz által állandó nyomáson végzett
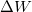 munka, a gázzal közölt
munka, a gázzal közölt 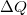 hőmennyiség és a
hőmennyiség és a 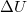 belső energia-változás között, ha a
belső energia-változás között, ha a 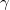 fajhőviszony ismert!Végeredmény
fajhőviszony ismert!Végeredmény![\[\Delta Q = \frac{\gamma}{\gamma-1}\Delta W = \gamma \Delta U\]](/images/math/8/5/b/85be9e56262f39a875414a126cad154e.png)
- Ha egy rendszert az ábrán látható 1 úton viszünk az
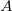 állapotból a
állapotból a 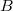 állapotba,
állapotba, 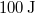 hőt vesz fel, miközben
hőt vesz fel, miközben 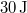 munkát végez.
munkát végez.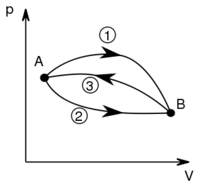
- a) Mennyi hőt vesz fel a rendszer az
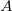 és
és 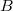 állapotok közt a 2 úton, ha közben
állapotok közt a 2 úton, ha közben 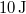 munkát végez?Végeredmény
munkát végez?Végeredmény![\[\Delta Q = 80\,\rm{J}\]](/images/math/5/c/e/5ce69d1df43da9c44332675f00e619cb.png)
- b) Ha
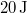 munkával vihetjük a rendszert
munkával vihetjük a rendszert 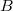 -ből
-ből 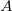 -ba a 3 út mentén, mennyi a közben leadott hő?Végeredmény
-ba a 3 út mentén, mennyi a közben leadott hő?Végeredmény![\[\Delta Q = 90\,\rm{J}\]](/images/math/0/8/c/08ce50a287cbb333107df509b4469cb7.png)
- a) Mennyi hőt vesz fel a rendszer az
- Mutassa meg, hogy ideális gáz izoterm összenyomásánál a kompresszibilitás
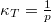 , míg adiabatikus összenyomásnál
, míg adiabatikus összenyomásnál 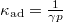 , ahol
, ahol 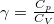 .ÚtmutatásHasználjuk a kompresszibilitás definícióját, és a megfelelő folyamatokat leíró egyenleteket.Végeredmény
.ÚtmutatásHasználjuk a kompresszibilitás definícióját, és a megfelelő folyamatokat leíró egyenleteket.Végeredmény![\[\kappa_{\mathit{ad}}=\frac{1}{\gamma p}\]](/images/math/1/f/e/1feb5ea49c75fe40f04869aa24729ef9.png)
- A
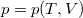 állapotegyenlet ismeretében fejezzük ki a
állapotegyenlet ismeretében fejezzük ki a 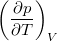 mennyiséget a
mennyiséget a 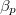 hőtágulási együttható és a
hőtágulási együttható és a 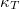 izotermikus kompresszibilitás segítségével!ÚtmutatásHasználja fel a két mennyiség definícióját és azt, hogy állandó nyomáson a
izotermikus kompresszibilitás segítségével!ÚtmutatásHasználja fel a két mennyiség definícióját és azt, hogy állandó nyomáson a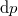 teljes differenciál nulla. Végeredmény
teljes differenciál nulla. Végeredmény![\[{\left(\frac{\partial p}{\partial T}\right)}_V = \frac{\beta_p}{\kappa_T}\]](/images/math/e/4/9/e496792ff87f32233de1607c8704883d.png)
- Egy
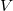 térfogatú szobában befűtünk. A szobában a hőmérséklet eközben állandó légköri nyomáson
térfogatú szobában befűtünk. A szobában a hőmérséklet eközben állandó légköri nyomáson  -ről
-ről 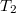 -re nő. Mennyivel változik a szobában lévő levegő belső energiája?VégeredményNem változik.
-re nő. Mennyivel változik a szobában lévő levegő belső energiája?VégeredményNem változik.
- Egy kezdetben
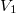 térfogatú,
térfogatú, 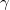 fajhőviszonyú ideális gáz térfogatát
fajhőviszonyú ideális gáz térfogatát 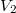 -re növeljük. A folyamatot egyszer adiabatikusan, másodszor pedig izotermikusan hajtjuk végre. Az első és második végállapotban a nyomások aránya
-re növeljük. A folyamatot egyszer adiabatikusan, másodszor pedig izotermikusan hajtjuk végre. Az első és második végállapotban a nyomások aránya 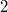 . Mekkora a
. Mekkora a 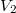 térfogat?Végeredmény
térfogat?Végeredmény![\[V_2=V_1\,2\frac{1}{\gamma-1}\]](/images/math/7/d/5/7d587d64171a43d070331fc0db59c195.png)
- Van der Waals-gázok belső energiájának térfogatfüggése az alábbi összefüggéssel adható meg: ahol
![\[ U = c_V mT - \frac{m^2}{M^2}\frac{a}{V},\]](/images/math/b/4/7/b47f383e5a17bd995a4937b18f1989c8.png)
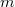 a gáz tömege,
a gáz tömege, 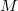 a móltömeg,
a móltömeg, 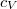 az állandó térfogaton mért fajhő,
az állandó térfogaton mért fajhő,  állandó.
állandó.
Egy hőszigetelt tartályt rögzített, jó hővezető anyagból készített fal választ két részre, amelyekbe azonos tömegű Van der Waals-gázt vezettünk be. A kezdeti állapotjellemzők: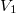 ,
,  , illetve
, illetve 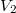 ,
, 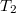 .
.
- a) Mennyi lesz a végső egyensúlyi hőmérséklet?Végeredmény
![\[T=\frac{T_1+T_2}{2}\]](/images/math/4/5/d/45d22e35974fa6f3871ee196153942fb.png)
- b) Hogyan módosul a válasz, ha a gáz betöltése után az elválasztó falat rögtön kivesszük?ÚtmutatásAlkalmazzuk az I. főtételt. A gáz fajhőjét tekintsük állandónak.Végeredmény
![\[T=\frac{T_1+T_2}{2}-\frac{ma\left(V_1-V_2\right)^2}{2M^2c_VV_1V_2\left(V_1+V_2\right)}\]](/images/math/7/9/5/795c653443761983b2ab64515717f29d.png)
- a) Mennyi lesz a végső egyensúlyi hőmérséklet?
- Kondenzált (folyadék vagy szilárd) anyagok egyik közelítő állapotegyenlete Mi az
![\[V= V_0(1-ap+bT).\]](/images/math/3/2/d/32dfd83af77dc0541a76a1b499f794f8.png)
 és
és 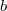 paraméterek jelentése?Végeredmény
paraméterek jelentése?Végeredmény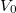 térfogatnál érvényes izotermikus kompresszibilitás és hőtágulási együttható.
térfogatnál érvényes izotermikus kompresszibilitás és hőtágulási együttható.
- Szilárd testek hőtágulási együtthatója, illetve izotermikus kompresszibilitása alacsony hőmérsékleten az alábbi összefüggésekkel adható meg: (
![\[ \beta_p = \frac{3aT^3}{V},\qquad \kappa_T=\frac{b}{V} \]](/images/math/c/4/5/c452cee6e528e707dc57f0f8a8cb00da.png)
 és
és 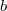 állandók). Határozzuk meg a szilárd test ilyenkor érvényes állapotegyenletét!ÚtmutatásIntegráljuk a fenti mennyiségek definíciós egyenletét!Végeredményahol
állandók). Határozzuk meg a szilárd test ilyenkor érvényes állapotegyenletét!ÚtmutatásIntegráljuk a fenti mennyiségek definíciós egyenletét!Végeredményahol![\[p=\frac{3a}{4b}T^4+\frac{V_0-V}{b},\]](/images/math/f/0/3/f03818c4d7f756ea3d47cd7ddb4bed96.png)
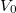 állandó.
állandó.
- Fejezzük ki a
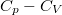 különbséget
különbséget 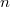 mol Van der Waals-gáz esetén a hőmérséklet, a térfogat és a
mol Van der Waals-gáz esetén a hőmérséklet, a térfogat és a 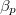 hőtágulási együttható segítségével!ÚtmutatásHasználjuk fel az általánosegyenletet, a Van der Waals-gáz belső energiájára vonatkozó összefüggést és a hőtágulási együttható definícióját.
hőtágulási együttható segítségével!ÚtmutatásHasználjuk fel az általánosegyenletet, a Van der Waals-gáz belső energiájára vonatkozó összefüggést és a hőtágulási együttható definícióját.![\[C_p-C_V=\frac{1}{n}\left(p+\left(\frac{\partial U}{\partial V}\right)_T\right)\left(\frac{\partial V}{\partial T}\right)_p\]](/images/math/c/3/4/c342b7595e6daf4375e0a9e1fafdf029.png) Végeredmény
Végeredmény![\[C_p-C_V=\frac{RT\beta_p}{1-nb/V}.\]](/images/math/a/7/4/a746f69df3bc690df6825fc3ea6c9d2d.png)
Fajhő, Körfolyamatok
- Melegszik vagy lehűl az
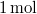 ideális gáz, ha a
ideális gáz, ha a 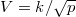 összefüggés (
összefüggés (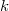 állandó) szerint tágul ki? Mekkora a gáz mólhője ebben a folyamatban, ha állandó térfogaton mért mólhője
állandó) szerint tágul ki? Mekkora a gáz mólhője ebben a folyamatban, ha állandó térfogaton mért mólhője 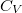 ?ÚtmutatásA fajhő általános definícióját használjuk, majd az állapotváltozás „pályáját” megadó egyenlet segítségével keressük meg a
?ÚtmutatásA fajhő általános definícióját használjuk, majd az állapotváltozás „pályáját” megadó egyenlet segítségével keressük meg a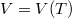 függvényt és abból a
függvényt és abból a 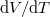 hányadost! VégeredményLehűl,
hányadost! VégeredményLehűl,![\[C=C_V-R\]](/images/math/9/1/6/916d05fdbb5dfa7f9b35fed114625c98.png)
- Határozzuk meg azon lehetséges folyamatokat megadó összefüggést, amelyek közben az ideális gáz mólhője állandó (az állandó nyomáson és állandó térfogaton mért mólhőket tekintsük ismertnek)! Vezessük le a kapott egyenletből az ismert, állandó mólhőjű speciális folyamatok egyenletét.ÚtmutatásAz első főtételbe írjuk be az állandónak feltételezett mólhőt, az állapotegyenlet segítségével küszböljük ki az egyenletből a hőmérsékletet, majd oldjuk meg a
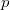 -re és
-re és 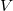 -re kapott differenciálegyenletet. Végeredmény
-re kapott differenciálegyenletet. Végeredmény![\[pV^\frac{C-C_p}{C-C_V}=\text{állandó}.\]](/images/math/0/8/4/0844c7b8571b41dceb34b69f2c02e722.png)
- Ideális gáz állapotváltozását a
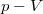 síkon a
síkon a 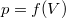 összefüggés írja le.
összefüggés írja le.
- a) Bizonyítsa be, hogy ebben a folyamatban a fajhő térfogatfüggését a összefüggés adja meg!
![\[c(V)=c_V+R\frac{f(V)}{f(V)+V\frac{\mathrm{d}f}{\mathrm{d}V}}\]](/images/math/9/5/f/95f7a48280858181d4b28ca447b3a9d2.png) ÚtmutatásA fejhő definíciós egyenletébe írjuk be a megadott függvényt, használjuk az állapotegyenletet és alkalmazzuk aösszefüggést!
ÚtmutatásA fejhő definíciós egyenletébe írjuk be a megadott függvényt, használjuk az állapotegyenletet és alkalmazzuk aösszefüggést!![\[\frac{\mathrm{d}V}{\mathrm{d}T}=\left(\frac{\mathrm{d}T}{\mathrm{d}V}\right)^{-1}\]](/images/math/c/8/8/c88d2444320e13642d1d1bc1085d8c92.png)
- b) Milyen
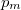 ,
, 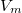 értékpárnál maximális a gáz hőmérséklete, ha az állapotváltozást a
értékpárnál maximális a gáz hőmérséklete, ha az állapotváltozást a 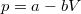 egyenlet adja meg (
egyenlet adja meg ( és
és 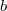 ismert pozitív állandók)?ÚtmutatásHasználjuk ki, hogy a maximális hőmérsékletnek megfelelő izoterma az állapotváltozást leíró görbe érintője, ahol a fajhőnek szingularitása van!Végeredmény
ismert pozitív állandók)?ÚtmutatásHasználjuk ki, hogy a maximális hőmérsékletnek megfelelő izoterma az állapotváltozást leíró görbe érintője, ahol a fajhőnek szingularitása van!Végeredmény![\[V_m=\frac{a}{2b}\qquad\text{és}\qquad p_m=\frac{a}{2}\]](/images/math/0/4/f/04f5f3e0fd92c07431c1162d1bfa547a.png)
- a) Bizonyítsa be, hogy ebben a folyamatban a fajhő térfogatfüggését a
- Az első ábrán egy ideális gázzal végzett körfolyamat
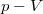 diagramja látható. Ábrázoljuk a folyamatot
diagramja látható. Ábrázoljuk a folyamatot 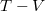 és
és 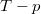 diagramon!
diagramon!
- A második ábrán egy ideális gázzal végzett körfolyamat
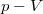 diagramja látható. Mekkora a gáz által végzett munka?
diagramja látható. Mekkora a gáz által végzett munka?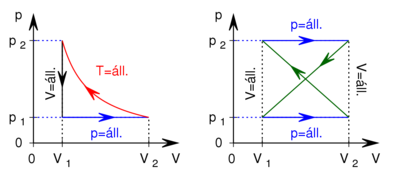 Végeredmény
Végeredmény![\[W=0.\]](/images/math/1/5/d/15d71ac95674055e4c06112ae5313e2d.png)
-
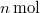 ,
, 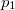 nyomású kétatomos ideális gázt
nyomású kétatomos ideális gázt 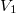 térfogatról állandó nyomáson
térfogatról állandó nyomáson 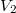 térfogatúra nyomunk össze (az ábrán 1-es út). Ezen az állandó térfogaton eredeti hőmérsékletére melegítjük (2-es út), majd izotermikusan a kiinduló térfogatára tágítjuk (3-as út).
térfogatúra nyomunk össze (az ábrán 1-es út). Ezen az állandó térfogaton eredeti hőmérsékletére melegítjük (2-es út), majd izotermikusan a kiinduló térfogatára tágítjuk (3-as út).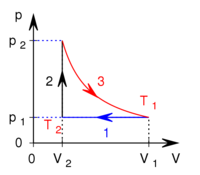
- a) Mennyivel változott a gáz belső energiája az 1-es úton?Végeredmény
![\[\Delta U_1 = p_1 \frac{V_2-V_1}{\gamma-1}, \qquad \gamma=\frac75\]](/images/math/2/f/6/2f69cad7cc3d66fb56085b61806960b8.png)
- b) Mennyivel hőt kellet közölnünk a gázzal a 2-es úton?Végeredmény
![\[\Delta Q_2=-\Delta U_1\]](/images/math/b/4/5/b45afb1d5d8899648966d216d44c756b.png)
- c) Mekkora a gáz által végzett munka és a gáz által felvett hő a teljes körfolyamatban?Végeredmény
![\[\Delta W = \Delta Q = p(V_2-V_1)+p_1V_1\ln\left(\frac{V_1}{V_2}\right)\]](/images/math/4/7/5/475bbd601cdf9182147bca5dfa9123cb.png)
- a) Mennyivel változott a gáz belső energiája az 1-es úton?
- Egy Carnot-hűtőgép egyik hőtartályában
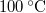 hőmérsékletű, forrásban lévő víz, a másikban
hőmérsékletű, forrásban lévő víz, a másikban 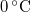 hőmérsékletű víz van. A víz forráshője
hőmérsékletű víz van. A víz forráshője 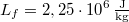 , a jég olvadáshője
, a jég olvadáshője 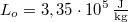 .
.
- a) Mennyi vizet kell az alsó hőtartályban
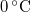 hőmérsékletű jéggé fagyasztani ahhoz, hogy a felső hőtartályban
hőmérsékletű jéggé fagyasztani ahhoz, hogy a felső hőtartályban 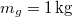 tömegű
tömegű 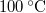 hőmérsékletű gőz keletkezzék?Végeredményahol
hőmérsékletű gőz keletkezzék?Végeredményahol![\[m_j=(1-\eta)L_f m_g/L_o=49{,}16\,\mathrm{kg},\]](/images/math/f/1/4/f147478a59f517a1b7dfabbe7bddefd5.png)
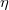 a körfolyamat hatásfoka.
a körfolyamat hatásfoka. - b) Mennyi külső munkát kell a körfolyamatba betáplálni?Végeredményahol
![\[W=\eta L_f m_g=6{,}03\cdot 10^5\,\mathrm{J},\]](/images/math/f/5/9/f59e5efd869a9a6687ee70f425700363.png)
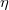 a körfolyamat hatásfoka.
a körfolyamat hatásfoka.
- a) Mennyi vizet kell az alsó hőtartályban
- Az ábrán a
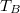 és
és 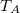 hőmérsékletekkel meghatározott körfolyamat látható. Mekkora annak a gépnek a hatásfoka, amelyik ezt a körfolyamatot mólnyi mennyiségű, adott
hőmérsékletekkel meghatározott körfolyamat látható. Mekkora annak a gépnek a hatásfoka, amelyik ezt a körfolyamatot mólnyi mennyiségű, adott 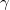 fajhőviszonyú ideális gázzal valósítja meg?
fajhőviszonyú ideális gázzal valósítja meg?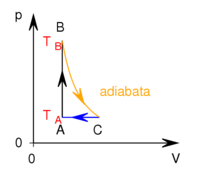 Végeredményahol
Végeredményahol![\[\eta=1-\gamma\frac{x^{1/gamma}-1}{x-1},\]](/images/math/e/e/c/eec4e9f8a52e569065ee348f1a0d0fad.png)
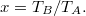
-
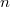 mólnyi ideális gáz az ábrán látható körfolyamatot végzi. A körfolymat két izobár és két adiabata szakaszból áll, amelyeket a
mólnyi ideális gáz az ábrán látható körfolyamatot végzi. A körfolymat két izobár és két adiabata szakaszból áll, amelyeket a 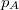 ,
, 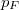 ,
, 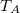 és
és 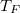 adatok határoznak meg (ez a gőzgép sémája).
adatok határoznak meg (ez a gőzgép sémája).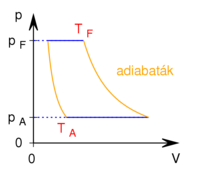
- a) Mekkora a gőzgép hatásfoka?
- b) Hogyan függ a hatásfok attól, hogy hány atomos gázmolekulákkal végezzük a körfolyamatot?
- c) Az adott gépnél és az adott gáznál hogyan növelhető a hatásfok?Végeredménya)
![\[\eta=1-\left(\frac{p_A}{p_F}\right)^{\frac{\gamma-1}{\gamma}}.\]](/images/math/b/0/6/b06b768320fb25e906c3a14c04833bbe.png)
b) A molekulák szabadsági fokának csökkentésével a hatásfok nő.
c) A nyomásviszony növelésévekl a hatásfok nő.
- Egy épület fűtésére az ún. dinamikus fűtést használjuk:
- A fűtőanyagot elégetjük egy hőerőgép tűzszekrényében, melynek hőmérsékletét állandó
 hőmérsékleten tartjuk (ez a hőerőgép felső hőtartálya).
hőmérsékleten tartjuk (ez a hőerőgép felső hőtartálya).
- A hőerőgép egy hőszivattyút működtet, amelynek alsó hőtartálya egy tó
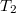 hőmérsékletű vize, felső hőtartálya pedig a hőerőgépet hűtő
hőmérsékletű vize, felső hőtartálya pedig a hőerőgépet hűtő  hőmérsékletű víz, amely az épületet egyúttal fűti (
hőmérsékletű víz, amely az épületet egyúttal fűti (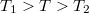 ).
).
- A tűzszekrényben
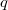 égéshőjű anyag ég, a hőerőgép és a hőszivattyú veszteség nélkül, Carnot-hatásfokkal működik. Határozzuk meg, mennyi hőt kap a helyiség egységnyi tömegű fűtőanyag elégetése árán!Végeredmény
égéshőjű anyag ég, a hőerőgép és a hőszivattyú veszteség nélkül, Carnot-hatásfokkal működik. Határozzuk meg, mennyi hőt kap a helyiség egységnyi tömegű fűtőanyag elégetése árán!Végeredmény![\[Q=q\frac{1-T_2/T_1}{1-T_2/T}>q.\]](/images/math/0/9/7/097b137e36faa49bbb8b3a3deaab5f04.png)
- A fűtőanyagot elégetjük egy hőerőgép tűzszekrényében, melynek hőmérsékletét állandó
Entrópia, II. főtétel
-
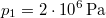 nyomású,
nyomású, 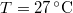 hőmérsékletű és
hőmérsékletű és 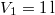 térfogatú ideális gáz izotermikusan
térfogatú ideális gáz izotermikusan 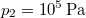 nyomásig terjed ki. Mennyivel változott meg eközben az entrópiája? ÚtmutatásHasználjuk az entrópiaváltozás definícióját és az állapotegyenletet!Végeredmény
nyomásig terjed ki. Mennyivel változott meg eközben az entrópiája? ÚtmutatásHasználjuk az entrópiaváltozás definícióját és az állapotegyenletet!Végeredmény![\[\Delta S=\frac{p_1 V_1}{T}\ln\frac{p_1}{p_2}=19{,}97\,\mathrm{\frac{J}{K}}\]](/images/math/6/d/0/6d0b864aa264a9c16325151512c98203.png)
- Mennyivel változik meg
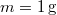 nitrogéngáz entrópiája, ha állandó nyomáson
nitrogéngáz entrópiája, ha állandó nyomáson 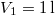 térfogatról
térfogatról 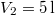 térfogatra expandáltatjuk.Végeredmény
térfogatra expandáltatjuk.Végeredmény![\[\Delta S=\frac{m}{\mu_\mathrm{N_2}}C_p\ln\frac{V_2}{V_1}=3{,}34\,\mathrm{\frac{J}{K}}, \qquad C_p=\frac72R.\]](/images/math/6/9/3/69379145baf5ca7bc790fdc4464b8173.png)
- Tekintsünk
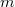 tömegű,
tömegű, 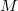 móltömegű,
móltömegű, 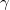 fajhőviszonyú ideális gázt.
fajhőviszonyú ideális gázt.
- a) Vezesse le az entrópia hőmérséklet- és térfogatfüggését megadó összefüggést!ÚtmutatásVizsgálja az entrópiaváltozást adiabatikus folyamatban!Végeredmény
![\[S=\frac{m}{M}R\ln\left(T^{\frac{1}{\gamma-1}}V\right)+S_0\]](/images/math/7/0/3/703497cb4e3daf33126d8a9df9ebb08d.png)
- b) A kapott entrópia-kifejezés segítségével vezesse le az adiabata egyenletét!ÚtmutatásVizsgálja az entrópiaváltozást adiabatikus folyamatban!Végeredmény
![\[TV^{\gamma-1}=\mathrm{const.}\]](/images/math/7/5/4/754140f6a21d584b63f5d26d9a18a297.png)
- a) Vezesse le az entrópia hőmérséklet- és térfogatfüggését megadó összefüggést!
- Az ideális gáz entrópiáját gyakran az
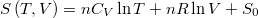 alakban használják.
alakban használják.
- a) Indokolja meg, hogy az
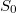 mennyiségnek függnie kell a rendszer anyagmennyiségét megadó
mennyiségnek függnie kell a rendszer anyagmennyiségét megadó 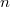 mólszámtól!VégeredményAz entrópia extenzív állapotjelző.
mólszámtól!VégeredményAz entrópia extenzív állapotjelző. - b) Adjon meg egy olyan
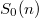 -függést, amellyel az entrópia fenti kifejezése teljesíti az a) pontban szereplő követelményt!Végeredményamivel az entrópia
-függést, amellyel az entrópia fenti kifejezése teljesíti az a) pontban szereplő követelményt!Végeredményamivel az entrópia![\[S_0(n)=-nR\ln n+ns_0,\]](/images/math/0/f/5/0f5e8e66063357f77affc5dd75e82760.png) ahol
ahol![\[S\left(T,V\right)=n C_V\ln T+nR\ln \frac{V}{n}+ ns_0,\]](/images/math/e/5/8/e580690ef414387f9272cc6ffe11e430.png)
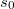 már
már 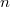 -től független.
-től független.
- a) Indokolja meg, hogy az
-
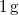
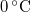 -os víz állandó nyomáson
-os víz állandó nyomáson 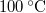 -os gőzzé alakul. Határozzuk meg a folyamat alatt bekövetkező entrópiaváltozást!.Végeredmény
-os gőzzé alakul. Határozzuk meg a folyamat alatt bekövetkező entrópiaváltozást!.Végeredmény![\[\Delta S = mc\ln\frac{373}{273}+\frac{mL_f}{373\,\mathrm{K}}=7{,}36\,\mathrm{\frac{J}{K}},\]](/images/math/8/f/f/8ff47ef68c48ff988ac413b430356235.png)
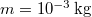 a víz tömege,
a víz tömege,  a víz fajhője,
a víz fajhője, 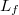 a forráshője.
a forráshője.
-
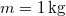 tömegű,
tömegű, 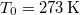 hőmérsékletű vizet termikus kapcsolatba hozunk egy
hőmérsékletű vizet termikus kapcsolatba hozunk egy 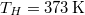 hőmérsékletű hőtartállyal.
hőmérsékletű hőtartállyal.
- a) Mekkora a víz entrópia-változása, miután a hőmérséklete elérte a hőtartály hőmérsékletét?Végeredmény
![\[1306\,\mathrm{\frac{J}{K}}\]](/images/math/2/d/8/2d8871a7637fa7346587bd1eb82a4c69.png)
- b) Mekkora eközben a hőtartály entrópia-változása?Végeredmény
![\[-1121\,\mathrm{\frac{J}{K}}\]](/images/math/0/3/9/039511937396c1ce27cf7b567a919c69.png)
- c) Mekkora a teljes rendszerben (hőtartály és víz) létrejött entrópia-változás?Végeredmény
![\[185\,\mathrm{\frac{J}{K}}\]](/images/math/0/6/1/06120b7dea96d50e3214e101a83a9563.png)
- d) Mennyi a teljes rendszerben létrejött entrópia-változás, ha a testet először egy
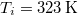 hőmérsékletű hőtartállyal, majd az egyensúly beállta után a
hőmérsékletű hőtartállyal, majd az egyensúly beállta után a 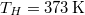 hőmérsékletű hőtartállyal hozzuk kapcsolatba?Végeredmény
hőmérsékletű hőtartállyal hozzuk kapcsolatba?Végeredmény![\[98\,\mathrm{\frac{J}{K}}\]](/images/math/9/2/9/929c0bc6fa4c0264edcf460bb60e5c28.png)
- e) Lehet-e úgy melegíteni a vizet, hogy a teljes rendszer entrópia-változása kisebb legyen egy előírt értéknél (vagyis a folyamat előírt mértékben megközelítse a reverzíbilis folyamatot)?VégeredményIgen.
- a) Mekkora a víz entrópia-változása, miután a hőmérséklete elérte a hőtartály hőmérsékletét?
- Tekintsünk ideális gázzal végzett Carnot-körfolyamatot.
- a) Ábrázoljuk a Carnot-körfolyamatot
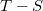 diagramban!
diagramban!
- b) Mutassuk ki, hogy a körfolyamatban a gáz által végzett munka most is a körfolyamat területével egyenlő!
- c) Számítsuk ki a fentiek alapján a Carnot-körfolyamat hatásfokát!
- a) Ábrázoljuk a Carnot-körfolyamatot
- Egymástól válaszfallal elzárt,
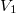 és
és 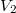 térfogatú két edényben azonos hőmérsékletű, azonos nyomású,
térfogatú két edényben azonos hőmérsékletű, azonos nyomású, 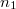 és
és 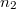 mólszámú, különböző fajtájú ideális gáz van. Ha a válaszfalat eltávolítjuk, akkor a két gáz összekeveredik.
mólszámú, különböző fajtájú ideális gáz van. Ha a válaszfalat eltávolítjuk, akkor a két gáz összekeveredik.
- a) Indokoljuk meg, hogy a folyamatban miért nem változik a hőmérséklet és a nyomás!VégeredményIdeális gázról van szó és érvényes a Dalton-törvény.
- b) Határozzuk meg az entrópia-változást (az ún. keverési entrópiát), és fejezzük ki a gázok
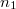 és
és 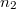 mólszámaival!ÚtmutatásAlkalmazzuk az Ideális gáz entrópiájáról szóló feladatban kapott entrópia-kifejezést, tegyük fel, hogy a teljes edényt kitöltő két gáz mindegyikének entrópiája úgy számítható, mintha a másik nem lenne jelen, és használjuk fel a Dalton-törvényt.Végeredmény
mólszámaival!ÚtmutatásAlkalmazzuk az Ideális gáz entrópiájáról szóló feladatban kapott entrópia-kifejezést, tegyük fel, hogy a teljes edényt kitöltő két gáz mindegyikének entrópiája úgy számítható, mintha a másik nem lenne jelen, és használjuk fel a Dalton-törvényt.Végeredmény![\[\Delta S = R n_1 \ln\frac{n_1+n_1}{n_1} + R n_2 \ln\frac{n_1+n_2}{n_2}\]](/images/math/5/9/6/596d530da1c94e91161150cb929bb191.png)
- c) Számítsuk ki az entrópia-változást, ha a két edényben azonos fajtájú gáz van!ÚtmutatásA levezetésnél vegyük figyelembe, hogy a keverés utáni állapotban az egész edényben ugyanaz a gáz van. A különböző gázokra levezetett fenti összefüggésből nem kapunk helyes eredményt; ez a Gibbs-féle paradoxon.Végeredmény
![\[\Delta S=0\]](/images/math/8/1/c/81ca578b10374e17bce8368f5500ff49.png)
- a) Indokoljuk meg, hogy a folyamatban miért nem változik a hőmérséklet és a nyomás!
-
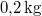 ,
, 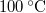 hőmérsékletű vasat hőszigetelt kaloriméterben lévő,
hőmérsékletű vasat hőszigetelt kaloriméterben lévő, 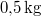 ,
, 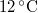 -os vízbe teszünk. A vas fajhője
-os vízbe teszünk. A vas fajhője 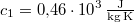 , a vízé
, a vízé 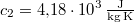 . Mennyi az entrópiaváltozás a hőmérséklet kiegyenlítődése miatt, ha a nyomás állandó?Végeredmény
. Mennyi az entrópiaváltozás a hőmérséklet kiegyenlítődése miatt, ha a nyomás állandó?Végeredmény![\[T_k=288{,}7\,\mathrm{K},\qquad \Delta S=3{,}41\,\mathrm{\frac{J}{K}}\]](/images/math/b/d/b/bdb4a99b8fe7577d94178ef75c691ba3.png)
- Két test azonos
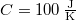 hőkapacitású, de hőmérsékletük különböző:
hőkapacitású, de hőmérsékletük különböző: 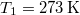 ,
, 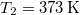 .
.
- a) Mennyi lesz a közös hőmérsékletük, ha termikus kapcsolatba hozzuk őket úgy, hogy a környezet felé ne legyen hőátadás?Végeredmény
![\[T_k=\frac{T_1+T_2}{2}\]](/images/math/e/4/0/e40444a3f717bb0150a6cddb411c076d.png)
- b) Mennyi lesz a közös hőmérséklet, ha a kiegyenlítődést egy reverzíbilisen működő hőerőgép végzi?Végeredmény
![\[T_k=\sqrt{T_1 T_2}\]](/images/math/2/2/5/22549fc9b794cce58ca4c0f18c2725c4.png)
- c) Ha a kiegyenlítődés nem jár térfogatváltozással, mekkora lesz a két esetben a belső energia megváltozása és az entrópia-változás?Végeredmény
![\[\Delta U_a=0, \qquad \Delta U_b=2C\sqrt{T_1 T_2}-CT_1-CT_2=-778{,}7\,\mathrm{J},\]](/images/math/4/4/a/44a431f68a2caaec70e8da0364f277ff.png)
![\[\Delta S_a=2C\ln\frac{T_1+T_2}{2}-C\ln T_1-C\ln T_2=2{,}42\,\mathrm{\frac{J}{K}}, \qquad \Delta S_b=0.\]](/images/math/7/a/1/7a11e8b14bc0459f04ada0abf724dd1b.png)
- a) Mennyi lesz a közös hőmérsékletük, ha termikus kapcsolatba hozzuk őket úgy, hogy a környezet felé ne legyen hőátadás?
Homogén rendszerek
- Bizonyítsuk be a
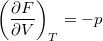 ,
, 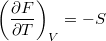 ,
, 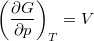 és
és 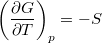 összefüggéseket!
összefüggéseket!
- Bizonyítsuk be a
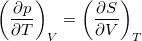 Maxwell-összefüggést!
Maxwell-összefüggést!
- Állandó anyagmennyiségű homogén rendszerben termikus és mechanikai kölcsönhatás esetén fennáll a
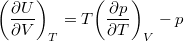 egyenlet. A fenti egyenlet levezetésének mintájára bizonyítsuk be, hogy ha a termikus kölcsönhatás mellett tetszőleges –
egyenlet. A fenti egyenlet levezetésének mintájára bizonyítsuk be, hogy ha a termikus kölcsönhatás mellett tetszőleges – 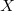 intenzív- és
intenzív- és 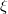 extenzív mennyiségpárral jellemzett – kölcsönhatás lép fel, akkor a fenti egyenlet érvényes marad, ha végrehajtjuk a
extenzív mennyiségpárral jellemzett – kölcsönhatás lép fel, akkor a fenti egyenlet érvényes marad, ha végrehajtjuk a 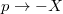 és a
és a 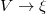 változócserét!
változócserét!
- Fejezzük ki mérhető mennyiségekkel (hőtágulási együttható, kompresszibilitás, mólhő) egy rendszer
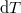 hőmérséklet-változását, ha térfogata adiabatikus, kvázisztatikus folyamat során
hőmérséklet-változását, ha térfogata adiabatikus, kvázisztatikus folyamat során 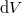 -vel megváltozik! Mutassuk meg, hogy
-vel megváltozik! Mutassuk meg, hogy 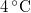 alatt a víz adiabatikus, kvázisztatikus összenyomáskor lehűl!ÚtmutatásÍrjuk fel az első főtételt, írjuk be az
alatt a víz adiabatikus, kvázisztatikus összenyomáskor lehűl!ÚtmutatásÍrjuk fel az első főtételt, írjuk be az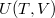 függvény teljes differenciálját, alkalmazzuk a belső energia térfogatfüggésére érvényes összefüggést, és a nyomás hőmérsékletfüggéséről szóló feladat eredményét! A víz hőtágulási együtthatója
függvény teljes differenciálját, alkalmazzuk a belső energia térfogatfüggésére érvényes összefüggést, és a nyomás hőmérsékletfüggéséről szóló feladat eredményét! A víz hőtágulási együtthatója 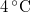 alatt negatív.
alatt negatív.
- Feltételezve, hogy
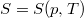 , mutassuk ki, hogy
, mutassuk ki, hogy 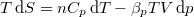 , ahol
, ahol 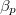 az izobár hőtágulási együttható.ÚtmutatásÍrjuk fel
az izobár hőtágulási együttható.ÚtmutatásÍrjuk fel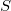 teljes differenciálját, használjuk a
teljes differenciálját, használjuk a 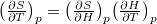 matematikai összefüggést, a termodinamika két differenciális összefüggését és a
matematikai összefüggést, a termodinamika két differenciális összefüggését és a 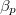 definícióját.
definícióját.
- Az első főtétel és a termodinamika differenciálegyenletei felhasználásával mutassuk meg, hogy ha ismerjük egy állandó anyagmennyiségű rendszer belső energiáját a térfogat és az entrópia függvényeként (vagyis az
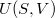 függvényt), akkor a rendszer bármely állapotjelzője (nyomás, hőmérséklet, entalpia, stb.) megadható
függvényt), akkor a rendszer bármely állapotjelzője (nyomás, hőmérséklet, entalpia, stb.) megadható 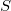 és
és 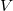 függvényeként!
függvényeként!
- Mennyivel változik egy
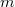 tömegű,
tömegű,  hőmérsékletű,
hőmérsékletű, 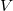 térfogatú rendszer entrópiája, ha térfogata állandó nyomáson
térfogatú rendszer entrópiája, ha térfogata állandó nyomáson 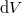 értékkel megnő? Az állandó nyomáson mért
értékkel megnő? Az állandó nyomáson mért 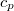 fajhőt és a
fajhőt és a 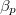 hőtágulási együtthatót ismertnek tekintjük.ÚtmutatásÍrjuk fel az
hőtágulási együtthatót ismertnek tekintjük.ÚtmutatásÍrjuk fel az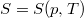 függvény teljes differenciálját állandó nyomáson, és alkalmazzuk
függvény teljes differenciálját állandó nyomáson, és alkalmazzuk 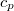 és
és 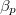 definícióját! Végeredmény
definícióját! Végeredmény![\[\mathrm{d}S=\frac{m c_p}{TV\beta_p}\,\mathrm{d}V\]](/images/math/8/9/1/8913482ffd0e5fd05a97ff4d3c990a0a.png)
- Egy rendszer állapotegyenlete
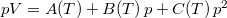 , ahol a hőmérsékletfüggő együtthatók kísérletekből ismertek. Mennyit változik a rendszer szabad entalpiája és entrópiája, ha a nyomást rögzített
, ahol a hőmérsékletfüggő együtthatók kísérletekből ismertek. Mennyit változik a rendszer szabad entalpiája és entrópiája, ha a nyomást rögzített  hőmérsékleten
hőmérsékleten 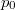 -ról
-ról 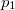 -re változtatjuk?ÚtmutatásHasználjuk ki a
-re változtatjuk?ÚtmutatásHasználjuk ki a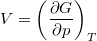 és az
és az 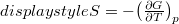 összefüggéseket! Végeredményés
összefüggéseket! Végeredményés![\[\Delta G=A\ln\left(\frac{p_1}{p_0}\right)+B\left(p_1-p_0\right)+C\frac{p_1^2-p_0^2}{2}\]](/images/math/6/0/4/604b4690f62d9f0616982b2cd9d8dfe5.png) ahol a vessző a hőmérséklet szerinti deriváltat jelenti.
ahol a vessző a hőmérséklet szerinti deriváltat jelenti.![\[\Delta S=A'\ln\left(\frac{p_1}{p_0}\right)+B'\left(p_1-p_0\right)+C'\frac{p_1^2-p_0^2}{2},\]](/images/math/9/4/d/94dc473377e76fb6ed5fbb18beabd15f.png)
- Egy gumiszalag állapotegyenlete
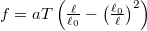 alakba írható, ahol
alakba írható, ahol 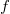 a szalagban fellépő húzóerő nagysága,
a szalagban fellépő húzóerő nagysága, 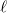 a szalag hossza,
a szalag hossza,  a hőmérséklet,
a hőmérséklet, 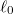 a szalag erőmentes hossza,
a szalag erőmentes hossza,  pozitív állandó.
pozitív állandó.
- a) Mutassuk ki, hogy a belső energia nem függ a szalag hosszától!ÚtmutatásA belső energia térfogatfüggésére kapott általános összefüggés átírható a vizsgált esetre a
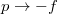 és
és 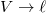 helyettesítéssel.
helyettesítéssel. - b) Írjuk fel a termodinamika fundamentális egyenletét, továbbá a szabad energia és a szabad entalpia megváltozását a gumiszalagra!ÚtmutatásAlkalmazzuk az a) pontban leírt fenti változócseréket!Végeredmény
![\[\mathrm{d}U=T\mathrm{d}S+f\mathrm{d}\ell\]](/images/math/7/f/5/7f5decf22c82e848373c1a93e96bafaf.png)
- c) Mekkora munkát végzünk, és mennyi a gumiszalag által leadott hő, ha a szalag hosszát izotermikus, reverzíbilis folyamatban
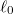 -ról
-ról 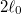 -ra növeljük.ÚtmutatásHasználjuk az I. főtételt, és vegyük figyelembe az a) részfeladat eredményét!Végeredmény
-ra növeljük.ÚtmutatásHasználjuk az I. főtételt, és vegyük figyelembe az a) részfeladat eredményét!Végeredmény![\[W=Q_\text{le}=\int_{\ell_0}^{2\ell_0}f\mathrm{d}\ell\]](/images/math/a/9/2/a92623436a83ffbf664f8f1a1b3458ef.png)
- d) Igazoljuk, hogy a gumiszalag hőmérséklete megnő, ha adiabatikusan megnyújtjuk!ÚtmutatásHasonlítsuk össze a fundamentális egyenletet és az
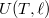 függvény teljes differenciálját, és vegyük figyelembe az (a) részfeladat eredményét! Végeredményahol
függvény teljes differenciálját, és vegyük figyelembe az (a) részfeladat eredményét! Végeredményahol![\[\left(\frac{\partial T}{\partial \ell}\right)_S=\frac{f}{C_\ell}>0,\]](/images/math/4/8/f/48fb10b34970193d78d5a4a66ee9c31c.png)
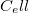 az állandó hossznál mért hőkapacitás.
az állandó hossznál mért hőkapacitás.
- a) Mutassuk ki, hogy a belső energia nem függ a szalag hosszától!
- Mennyi hő szabadul fel az
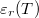 dielektromos állandójú dielektrikum polarizációjakor, ha a külső elektromos tér nagyságát állandó hőmérsékleten, kvázi-stacionáriusan növeljük nulláról egy nem túl nagy
dielektromos állandójú dielektrikum polarizációjakor, ha a külső elektromos tér nagyságát állandó hőmérsékleten, kvázi-stacionáriusan növeljük nulláról egy nem túl nagy 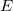 értékre? A térfogatváltozás elhanyagolható.ÚtmutatásHasználjuk az I. főtétel
értékre? A térfogatváltozás elhanyagolható.ÚtmutatásHasználjuk az I. főtétel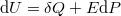 alakját, az
alakját, az 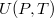 függvény teljes differenciálját, és azt, hogy a belső energia térfogatfüggésére kapott általános összefüggés átírható erre az esetre is a dielektrikum teljes dipólusmomentuma (
függvény teljes differenciálját, és azt, hogy a belső energia térfogatfüggésére kapott általános összefüggés átírható erre az esetre is a dielektrikum teljes dipólusmomentuma (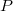 ) segítségével a
) segítségével a  és
és  helyettesítéssel:
helyettesítéssel: 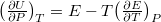 . Alkalmazzuk még a
. Alkalmazzuk még a 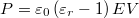 összefüggést is! Végeredmény
összefüggést is! Végeredmény![\[Q=-\frac12T\varepsilon_0V\frac{\mathrm{d}\varepsilon_r(T)}{\mathrm{d}T}E^2\]](/images/math/7/4/8/748a2556baf501bef94eaf7c54b03a77.png)
Fázisátalakulások
- Mutassuk meg, hogy mechanikai- és termikus kölcsönhatásban részt vevő rendszerben állandó nyomáson végbemenő fázisátalakulásnál az átalakulási hő (
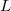 ) az entalpiaváltozással (
) az entalpiaváltozással (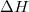 ) egyenlő!ÚtmutatásHasználjuk az entalpia definícióját és az első főtételt!
) egyenlő!ÚtmutatásHasználjuk az entalpia definícióját és az első főtételt!
-
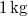 víznek normál nyomáson (
víznek normál nyomáson (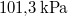 ) való elforralásához egy elektromos merülőforralón a
) való elforralásához egy elektromos merülőforralón a 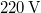 -os feszültségforrásból
-os feszültségforrásból 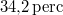 -en át
-en át 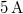 áramot kell átfolyatni. A gázállandó
áramot kell átfolyatni. A gázállandó 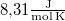 , a víz moláris tömege
, a víz moláris tömege 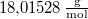 .
.
Határozzuk meg a víz- a) entalpia-,Útmutatáshasználjuk fel az előző feladat eredményét az izobár átalakulási hőre.Végeredmény
![\[\Delta H = W_\text{el} = 2{,}26\,\mathrm{MJ}\]](/images/math/4/f/d/4fdaf5770143071de6a318dd403592b3.png)
- b) entrópia- ésÚtmutatáshasználjuk az entrópia definíciójátVégeredmény
![\[\Delta S = 6{,}06\,\mathrm{\frac{kJ}{K}}\]](/images/math/7/2/7/7276d2981b6be7939e2cbb7053cfb7e9.png)
- c) belső energiaváltozását ebben a folyamatban!Útmutatásírjuk fel az entalpiaváltozás és belső energiaváltozás összefüggését, hanyagoljuk el a víz térfogatát a gőzéhez képest, és a gőzt tekintsük ideális gáznak.Végeredmény
![\[\Delta U=\Delta H-\frac{m}{M}RT=2{,}09\,\mathrm{MJ}\]](/images/math/0/8/9/089fe9b22dd39aba913ca295f3f5cd56.png)
- a) entalpia-,
- Henger alakú edényben
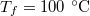 hőmérsékletű telített vízgőz van. Egy súlytalan dugattyú lassú betolásának hatására az edényben
hőmérsékletű telített vízgőz van. Egy súlytalan dugattyú lassú betolásának hatására az edényben 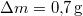 víz lecsapódik. A víz moláris tömege
víz lecsapódik. A víz moláris tömege 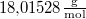 A folyamat során a nyomás a
A folyamat során a nyomás a 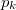 külső légnyomással egyenlő.
külső légnyomással egyenlő.
Mennyi munkát végeztünk ezalatt az ideális gáznak tekinthető vízgőzön?Végeredmény![\[\Delta W=p_k\left(V_1-V_2\right)=\frac{RT_f}{M}\Delta m=120\,\mathrm{J}\]](/images/math/0/1/c/01c0c0abb9f739cbff493a96bc03ec39.png)
- Ábrázoljuk (kvalitatív módon) egy tiszta anyag kémiai potenciáljának
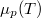 hőmérsékletfüggését állandó nyomáson, az anyag szilárd-, folyadék- és gőzállapotát átfogó hőmérséklet-intervallumban! Az olvadáspontot
hőmérsékletfüggését állandó nyomáson, az anyag szilárd-, folyadék- és gőzállapotát átfogó hőmérséklet-intervallumban! Az olvadáspontot 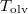 -val, a forráspontot
-val, a forráspontot 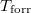 -ral jelöljük, és tegyük fel, hogy a mólentrópia egy fázison belül nem függ a hőmérséklettől!ÚtmutatásHasználjuk fel aegyenletet, a kémiai potenciál és a szabad entalpia összefüggését, továbbá két fázis egyensúlyának feltételét.
-ral jelöljük, és tegyük fel, hogy a mólentrópia egy fázison belül nem függ a hőmérséklettől!ÚtmutatásHasználjuk fel aegyenletet, a kémiai potenciál és a szabad entalpia összefüggését, továbbá két fázis egyensúlyának feltételét.![\[\left(\frac{\partial G}{\partial T}\right)_p=-S\]](/images/math/5/d/3/5d3e0ea157a966637bfd4bc7513fc8bd.png)
- Felhasználva, hogy az olvadáspont az állandó nyomáson felvett
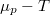 diagramban a szilárd fázisra és a folyadékra érvényes görbék metszéspontjánál van mutassuk ki, hogy a nyomás növelésekor az olvadáspont nő, ha a szilárd fázis móltérfogata kisebb, mint a folyadéké! Hogyan változik a jég olvadáspontja, a nyomás növelésekor?ÚtmutatásA nyomásváltozás a
diagramban a szilárd fázisra és a folyadékra érvényes görbék metszéspontjánál van mutassuk ki, hogy a nyomás növelésekor az olvadáspont nő, ha a szilárd fázis móltérfogata kisebb, mint a folyadéké! Hogyan változik a jég olvadáspontja, a nyomás növelésekor?ÚtmutatásA nyomásváltozás a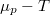 görbét eltolja, mégpedig a két fázisban általában különbözőképpen. A görbe eltolódásának mértékét adott hőmérsékleten, adott fázisban a összefüggés adja meg.
görbét eltolja, mégpedig a két fázisban általában különbözőképpen. A görbe eltolódásának mértékét adott hőmérsékleten, adott fázisban a összefüggés adja meg.![\[\left(\frac{\partial \mu }{\partial p}\right)_T= V_M\]](/images/math/2/5/a/25a4030c915d37e859e677c758ddfc3f.png)
- A szilárd-folyadék egyensúlyi görbének (olvadási görbe) közelítő meghatározására gyakran használják a
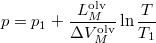 összefüggést (
összefüggést ( a
a 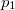 nyomáson,
nyomáson,  a
a 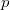 nyomáson érvényes olvadáspont, az egyenletben szereplő
nyomáson érvényes olvadáspont, az egyenletben szereplő 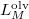 az anyag moláris átalakulási hője (vagy moláris entalpiaváltozása),
az anyag moláris átalakulási hője (vagy moláris entalpiaváltozása), 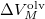 pedig a móltérfogat változása az olvadásnál).
pedig a móltérfogat változása az olvadásnál).
- a) Vezessük le ezt az egyenletet, és állapítsuk meg, hogy milyen feltételek mellett érvényes!ÚtmutatásIntegráljuk a Clausius-Clapeyron-egyenletet!
- b) Mutassuk ki, hogy a
 -hez képest kis
-hez képest kis 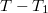 érték eseten az egyensúlyi nyomás lineárisan változik a
érték eseten az egyensúlyi nyomás lineárisan változik a 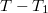 különbséggel!ÚtmutatásHasználjuk fel a kis
különbséggel!ÚtmutatásHasználjuk fel a kis -ekre érvényes
-ekre érvényes 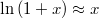 összefüggést.
összefüggést.
- a) Vezessük le ezt az egyenletet, és állapítsuk meg, hogy milyen feltételek mellett érvényes!
- A jég olvadáshője
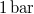 nyomáson
nyomáson 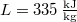 . A jég és a víz fajlagos térfogatának aránya
. A jég és a víz fajlagos térfogatának aránya 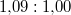 . Becsüljük meg, mennyivel tolódik el az olvadáspont kis nyomásnövekedés hatására!Végeredmény
. Becsüljük meg, mennyivel tolódik el az olvadáspont kis nyomásnövekedés hatására!Végeredmény![\[\mathrm{d}T=-\frac{0{,}09v_\text{víz}T}{L}\,\mathrm{d}p= -7{,}34\cdot10^{-8}\mathrm{\frac{K}{Pa}}\,\mathrm{d}p\]](/images/math/2/b/7/2b73b88d36a28976c45ec8366c83d6ee.png)
- Ha a nyomást
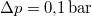 -ral megnöveljük, akkor a víz forrási hőmérséklete
-ral megnöveljük, akkor a víz forrási hőmérséklete 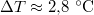 -kal növekszik. Ennek felhasználásával becsüljük meg a víz forráshőjét!ÚtmutatásA vízgőzre alkalmazzuk az ideális gáz egyenletét, és hanyagoljuk el a víz fajlagos térfogatát a gőzéhez képest!Végeredmény
-kal növekszik. Ennek felhasználásával becsüljük meg a víz forráshőjét!ÚtmutatásA vízgőzre alkalmazzuk az ideális gáz egyenletét, és hanyagoljuk el a víz fajlagos térfogatát a gőzéhez képest!Végeredmény![\[L_f\approx \frac{\Delta p}{\Delta T}\frac{RT^2}{p_kM}=2253\,\mathrm{\frac{kJ}{kg}}\]](/images/math/4/c/7/4c7c0dfc446c66a05097776d64fc920c.png)
- A szilárd argon
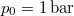 nyomáson
nyomáson 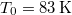 hőmérsékleten olvad meg. Olvadáshője ekkor
hőmérsékleten olvad meg. Olvadáshője ekkor 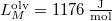 , móltérfogatának változása
, móltérfogatának változása 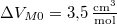 . A nyomás növekedésekor kísérleti eredmények szerint az olvadáshő nem változik, a
. A nyomás növekedésekor kísérleti eredmények szerint az olvadáshő nem változik, a 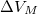 móltérfogatváltozás viszont az abszolút hőmérséklet megközelítőleg
móltérfogatváltozás viszont az abszolút hőmérséklet megközelítőleg 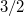 -ik hatványával arányos.
-ik hatványával arányos.
Mekkora nyomást kell alkalmaznunk ahhoz, hogy az olvadási hőmérséklet megkétszereződjék?ÚtmutatásA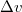 hőmérsékletfüggésének figyelembevételével integráljuk a Clausius-Clapeyron-egyenletet! Végeredmény
hőmérsékletfüggésének figyelembevételével integráljuk a Clausius-Clapeyron-egyenletet! Végeredmény![\[p=p_0+\frac{2L}{3\Delta v_0}\left(1-\left(\frac{T_0}{T}\right)^{3/2}\right)=1449\,\mathrm{bar}\]](/images/math/b/5/9/b59affbd1e174e38c0177e77ed696768.png)
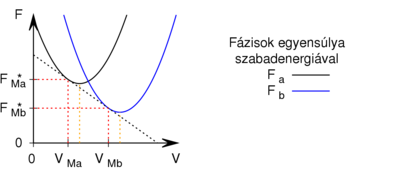
- Egy homogén anyag adott hőmérsékleten két fázisban (
 és
és 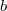 ) létezhet. Az egyes fázisok moláris szabad energiáinak térfogattól való függése (rögzített hőmérsékleten, állandó anyagmennyiség esetén) az ábrán látható.
) létezhet. Az egyes fázisok moláris szabad energiáinak térfogattól való függése (rögzített hőmérsékleten, állandó anyagmennyiség esetén) az ábrán látható.
Mutassuk ki, hogy egyensúlyi állapotban a fázisok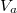 és
és 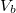 térfogatai a két görbéhez húzott közös érintő érintési pontjainak abszcisszái, a közös nyomás pedig az érintő negatív iránytangense!Útmutatásfejezzük ki a nyomást és a kémiai potenciált a szabad energiával (
térfogatai a két görbéhez húzott közös érintő érintési pontjainak abszcisszái, a közös nyomás pedig az érintő negatív iránytangense!Útmutatásfejezzük ki a nyomást és a kémiai potenciált a szabad energiával (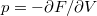 , ill.
, ill. 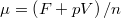 ), és használjuk ki, hogy fázisegyensúlyban a két fázis nyomása és kémiai potenciálja egyenlő!
), és használjuk ki, hogy fázisegyensúlyban a két fázis nyomása és kémiai potenciálja egyenlő!
- Az ábrán különböző mennyiségek hőmérsékletfüggését mutatjuk be a
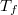 fázisátalakulási hőmérséklet környezetében. Az ábrák közül melyik tartozhat elsőrendű és melyik másodrendű fázisátalakuláshoz?
fázisátalakulási hőmérséklet környezetében. Az ábrák közül melyik tartozhat elsőrendű és melyik másodrendű fázisátalakuláshoz?

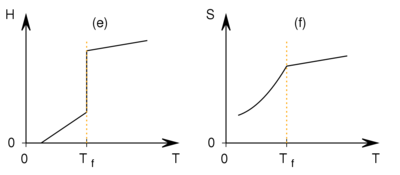
 VégeredményElsőrendűek: a), b), e), h).
VégeredményElsőrendűek: a), b), e), h).
Másodrendűek: c)', d)', f), g).
Kvantummechanikai bevezető
- Nyári napsütésben, délben a Föld felszínének
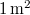 -én átlagosan kb.
-én átlagosan kb. 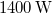 napsugárzási teljesítmény mérhető. Becsüljük meg a Nap felszínének hőmérsékletét!
napsugárzási teljesítmény mérhető. Becsüljük meg a Nap felszínének hőmérsékletét!
(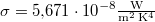 )ÚtmutatásHasználjuk ki, hogy a Nap által kibocsátott összes sugárzási teljesítmény egyenletesen oszlik el egy földpálya sugarú gömbfelületen.Végeredmény
)ÚtmutatásHasználjuk ki, hogy a Nap által kibocsátott összes sugárzási teljesítmény egyenletesen oszlik el egy földpálya sugarú gömbfelületen.Végeredmény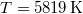
- Egy izzólámpában a volfrámszál hőmérséklete kb.
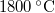 . Az emberi szem a
. Az emberi szem a 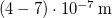 hullámhossz tartományban lát. Becsülje meg az izzólámpa „hatásfokát”!ÚtmutatásHasználja a Planck-féle sugárzási törvényt, a látható intervallumban alkalmazzon közelítést.Végeredmény
hullámhossz tartományban lát. Becsülje meg az izzólámpa „hatásfokát”!ÚtmutatásHasználja a Planck-féle sugárzási törvényt, a látható intervallumban alkalmazzon közelítést.Végeredmény![\[\frac{\Delta \mathcal{E}}{\mathcal{E}_t}=0{,}355\%\]](/images/math/e/a/1/ea1bc4434817421fb132a20eb6e23fd8.png)
- Határozzuk meg, hogy egy
 hőmérséklet fekete test milyen foton-áramsűrűséggel sugároz!ÚtmutatásA Planck-féle sugárzási törvényben különítse el a foton energiáját.Végeredmény
hőmérséklet fekete test milyen foton-áramsűrűséggel sugároz!ÚtmutatásA Planck-féle sugárzási törvényben különítse el a foton energiáját.Végeredmény![\[N = 2{,}404 \frac{8\pi}{c^2}\left(\frac{kT}{h}\right)^3\]](/images/math/5/2/5/525d3b6c79fc0b7e9c3c5bc6bbcf4e34.png)
- Egy
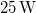 -os megfelelő gázzal töltött lámpától
-os megfelelő gázzal töltött lámpától 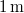 -re egy tantál fémfelületet (
-re egy tantál fémfelületet (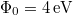 ) helyezünk el. A klasszikus elmélet alapján becsülje meg, hogy egy elektron átlagosan mennyi idő alatt gyűjtene össze annyi energiát, amivel kiléphet a fémből!
) helyezünk el. A klasszikus elmélet alapján becsülje meg, hogy egy elektron átlagosan mennyi idő alatt gyűjtene össze annyi energiát, amivel kiléphet a fémből!
(A valóságban a fotoeffektus során az elektronok a megvilágításkor „azonnal” kilépnek a fémből.)ÚtmutatásHasználja fel, hogy az izzó által kibocsátott összes sugárzási teljesítmény egyenletesen oszlik el az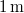 sugarú gömbfelületen. Végeredmény
sugarú gömbfelületen. Végeredmény![\[\Delta t= \frac{16\Phi_0}{P} \left( \frac{\ell}{D_\mathrm{Ta}} \right)^2 = 4{,}88\,\mathrm{s}\]](/images/math/a/9/0/a90e4994c9b40edbfb9deab6614d74db.png)
- Határozza meg, hogy a Compton-szórás esetén a beeső foton energiájának hány százalékát adja le az elektronnak!ÚtmutatásA Compton-szórás levezetéséhez írja fel a relativisztikus energia- és impulzusmegmaradást.Végeredményahol
![\[\eta = 1 - \left(\frac{p_f(1-\cos\vartheta)}{m_e c}+1\right)^{-1},\]](/images/math/e/3/d/e3d6a9c5338b3763b4cad5550a858ae6.png)
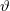 a foton eltérülése eredeti irányától.
a foton eltérülése eredeti irányától.
- Vizsgáljuk meg, hogy létezik-e olyan effektus, hogy egy szabad elektron teljes egészében elnyel egy fotont (teljesen rugalmatlan ütközés)! Ennek fényében, hogyan magyarázható a fotoeffektus?ÚtmutatásVizsgálja meg milyen körülmények között jöhetne létre Compton-szórás szabad elektronra.VégeredménySzabad elektronra nem létezik. Fotoeffektusnál az energiamegmaradásban figyelembe kell venni a kilépési munkát.
- Alkalmazza a Bohr–Sommerfeld-féle kvantálási hipotézist körpályán mozgó elektronra és egy lineáris oszcillátorra! Magyarázza meg a szupravezetésnél fellépő „fluxuskvantálás” jelenségét a Bohr–Sommerfeld-féle kvantálási hipotézis segítségével!ÚtmutatásÍrja fel és „kvantálja” a fázistérbeli pályaintegrált!VégeredményKörpályán mozgó elektronra
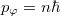 , lineáris oszcillátorra
, lineáris oszcillátorra 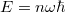 .
.
- Számítsa ki a hidrogénatom Bohr-féle modelljében a „körpályán” keringő elektron pályasugarát, sebességét, perdületét és energiáját!ÚtmutatásÍrja fel a körpályán tartó Coulomb-erőt és alkalmazza a kvantumhipotézist!Végeredmény
![\[ v_n = \frac{v_0}{n}, \qquad r_n = a_0 n^2,\]](/images/math/b/e/f/befdf1be2cd0570bc1714f3c8617241f.png) ahol
ahol![\[L_n = n\hbar, \qquad E_n = -\frac{E_0}{n^2}, \]](/images/math/f/b/6/fb6b76901bce25c085edd4b2973f8e77.png)
![\[v_0 = \frac{e^2}{4\pi\varepsilon_0\hbar}, \qquad a_0 = \frac{\hbar^2 4 \pi \varepsilon_0}{m_e e^2}, \]](/images/math/4/9/9/4999909021a110d647609282a1008127.png)
![\[ E_0 = \frac{m_e e^4}{2\hbar^2(4\pi\varepsilon_0)^2}.\]](/images/math/e/3/2/e3286e30266aeb2eb0d27f902ea46e8c.png)
- Számítsa ki, hogy a hidrogénatom Bohr-féle modelljében a relativisztikus tömegnövekedés milyen korrekciót jelentene az energiaszintekben!ÚtmutatásFejtse sorba a relativisztikus tömeget.Végeredmény
![\[ E_n = -\frac{E_0}{n^2}-\frac{E_0}{2} \frac{\alpha_f^2}{n^4}+O\left[n^{-6}\right], \]](/images/math/1/9/9/199cedfdb000e94b97da397355f62e91.png)
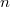 -ben negyedrendű korrekciót kapunk. Megjegyzendő, hogy az együttható nem pontos, mert a klasszikus relativisztikus tárgyalás nem juthat el arra a helyes eredményre, ami a kvantummechanikában a Klein–Gordon-formula néven ismert.
-ben negyedrendű korrekciót kapunk. Megjegyzendő, hogy az együttható nem pontos, mert a klasszikus relativisztikus tárgyalás nem juthat el arra a helyes eredményre, ami a kvantummechanikában a Klein–Gordon-formula néven ismert.
- Számítsa ki, hogy a hidrogénatom Bohr-féle modelljében a mag véges nagyságú tömege milyen korrekciót jelentene az energiaszintekben és a spektrumban!ÚtmutatásOldja meg a Bohr-modellt tömegközépponti koordináta-rendszerben.Végeredmény
![\[E_n^* = -\frac{E_0}{n^2},\]](/images/math/6/e/e/6ee9b65a150eb583861a491351b3a4f1.png) ahol
ahol![\[ E_0^* = \frac{E_0}{1+\textstyle \frac{m_e}{M}} \approx E_0 \left(1- \frac{m_e}{M}\right), \]](/images/math/3/c/f/3cfa608d96f63f174a55fb8b88a36a1c.png)
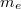 az elektron,
az elektron, 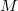 pedig az atommag tömege.
pedig az atommag tömege.
- Határozza meg, hogy az atomok fotonkibocsátásakor fellépő visszalökődés milyen korrekciót jelent az emissziós spektrumban!ÚtmutatásAlkalmazza az energia- és az impulzusmegmaradás tételét.VégeredményAz új frekvenciaahol
![\[\nu' \approx \frac{\nu}{1+\displaystyle \frac{h\nu}{Mc^2}},\]](/images/math/b/3/4/b3456225f815bfd0b26120dce20131a2.png)
 a visszalökődés nélküli foton frekvenciája,
a visszalökődés nélküli foton frekvenciája, 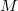 az atom tömege.
az atom tömege.
- Mutassa meg, hogy miként teljesül a „korrespondencia-elv” a hidrogénatom Bohr-féle modelljében a fénykibocsátása esetén!ÚtmutatásVizsgálja a hidrogénatom magasan gerjesztett állapotai közti átmeneteket.
- Hasonlítsa össze a foton és az elektron kinetikus energia-hullámszám görbéjét! Elemezze a lehetséges jellegzetességeket relativisztikus, és nemrelativisztikus esetekben!ÚtmutatásA relativisztikus összenergia
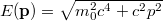 .
.
- Határozza meg a Schrödinger-féle hidrogénatomban az elektron alapállapoti hullámfüggvényét! Számítsa ki, hogy protontól milyen távolságban található meg az elektron a legnagyobb valószínűséggel!ÚtmutatásAz elektron sugárirányú megtalálási valószínűségének eloszlás
![\[ R(r) = A_n \left(\frac{r}{a_0}\right)^{n-1} e^{\textstyle -\frac{r}{n a_0}}.\]](/images/math/c/0/f/c0f960f3b75cc266fda2e137a4acc04b.png) Végeredmény
Végeredmény![\[r_\text{lv.}=n^2 a_0\]](/images/math/b/a/7/ba7a51917aa422072b054ff3f54a2da0.png)